Phaseolus vulgaris - haricot sec (PROTA)
Introduction |
| Importance générale | |
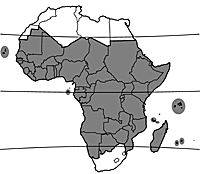
| Répartition en Afrique | |
| Répartition mondiale | |
| Céréale / légume sec | |
| Légume | |
| Médicinal | |
| Fourrage | |
| Auxiliaire | |
| Sécurité alimentaire | |
Phaseolus vulgaris L. - haricot sec
- Protologue : Sp. pl. 2: 723 (1753).
- Famille : Papilionaceae (Leguminosae - Papilionoideae, Fabaceae)
- Nombre de chromosomes : 2n = 22
Noms vernaculaires
- Haricot commun, haricot (Fr).
- Common bean, haricot bean, kidney bean, navy bean (En).
- Feijão, feijoeiro (Po).
- Mharagwe (Sw).
Origine et répartition géographique
Le haricot commun est originaire d’Amérique centrale et d’Amérique du Sud. Des écotypes à petites graines et à port grimpant se trouvent à l’état sauvage au nord de l’Argentine et en Amérique centrale. Le haricot commun a été domestiqué indépendamment en Amérique centrale (Mexique et Guatemala) et dans les Andes d’Amérique du Sud (principalement le Pérou). Les pools géniques qui en résultent sont distincts. Des preuves archéologiques indiquent que le haricot commun était déjà une plante domestiquée en 6000 avant J.-C au Pérou et en 5000 avant J.-C. au Mexique. Le haricot commun a été transporté vers d’autres continents depuis le XVIe siècle. Des marchands portugais ont probablement introduit le haricot commun en Afrique à partir du XVIe siècle, via Sofala (Mozambique), Zanzibar et Mombasa, d’où il a été diffusé vers des altitudes plus élevées à l’intérieur par des caravanes d’esclaves et des marchands. Le haricot commun s’est bien établi en tant que légume sec dans certaines régions d’Afrique avant l’ère coloniale. La diversité génétique de la plante et de ses agents pathogènes, ainsi que des preuves linguistiques, indiquent que le haricot commun est devenu une culture essentielle d’abord dans les régions d’altitude de l’Afrique centrale (par ex. au Rwanda et au Burundi) avant les autres régions d’Afrique.
De nos jours, il a une importance mondiale, en particulier en Amérique du Nord et du Sud, en Europe et en Afrique. L’espèce est bien établie dans de nombreux pays africains, mais c’est dans la région des Grands Lacs d’Afrique centrale que sa culture est la plus intensive. En Afrique tropicale, le haricot commun est une culture vivrière aussi importante pour les zones urbaines que rurales.
Usages
Les graines mûres sèches du haricot commun sont consommées comme légume sec dans le monde entier ; ses gousses et graines immatures se mangent comme légume. En Afrique tropicale, le haricot est produit et consommé avant tout comme légume sec. La valeur nutritionnelle de ses graines est reconnue, mais le haricot compte aussi pour la variété et le goût qu’il apporte à des mets riches en glucides, comme ceux à base de maïs ou de banane. Il constitue la principale source de protéines dans différents pays comme le Rwanda, le Burundi et le Kenya. Si le haricot est parfois désigné comme la “viande du pauvre”, il est aussi apprécié par des consommateurs plus riches. En Afrique tropicale, le haricot se consomme classiquement cuit à l’eau, souvent avec un assaisonnement et un peu d’huile. On peut aussi en faire des purées ou des soupes. En de nombreux endroits du monde, les graines sèches de haricot sont mises en conserve, soit nature, soit à la sauce tomate.
Les feuilles de haricot se consomment parfois comme légume, par ex. pendant les mois de disette lorsqu’on trouve peu à manger, mais il existe relativement peu de cultivars dont les feuilles sont suffisamment tendres. Les résidus de la plante servent souvent de fourrage. Au Mali, la poudre de graines carbonisées est appliquée sur les blessures.
Dans les zones tempérées du monde, Phaseolus vulgaris est surtout cultivé pour ses gousses immatures (haricot vert), que l’on conserve appertisées ou surgelées ou qui se mangent fraîches. En Afrique tropicale, les haricots verts sont une production essentiellement destinée à la vente. Un article distinct de PROTA 2 : “Légumes” traite de Phaseolus vulgaris en tant que légume.
Production et commerce international
Il est difficile de se procurer des statistiques fiables sur le haricot commun sec car sa production est souvent agrégée à celle des autres espèces de Phaseolus. En 2000, la production annuelle mondiale de haricot a été estimée par la FAO à 8,3 millions de t ; le plus gros producteur est le Brésil. L’Afrique produit environ 2 millions de t par an sur environ 3,5 millions d’ha. Les gros producteurs d’Afrique tropicale (100 000–600 000 ha par an) sont la R.D. du Congo, le Rwanda, le Burundi, l’Ethiopie, le Kenya, l’Ouganda, la Tanzanie, le Malawi, l’Angola et le Mozambique ; les petits producteurs (2000–100 000 ha) sont le Cap-Vert, le Niger, le Cameroun, le Soudan, la Zambie et le Zimbabwe. La plus grande part des haricots secs produits en Afrique tropicale est autoconsommée, mais 40% peuvent être commercialisés et approvisionnent les zones urbaines et l’export, ce qui représente une valeur d’US$ 200 millions par an payée au producteur. Les échanges commerciaux avec les pays voisins sont importants. Par exemple, des quantités notables passent de l’Ouganda au Kenya, au Rwanda et au Soudan ; ce qui n’empêche pas l’Ouganda d’en importer éventuellement de ces pays lorsque des déficits se présentent ici et là. Un exemple de commerce de haricots sur de longues distances est le transport entre le Kivu (à l’est de la R.D. du Congo) et Kisangani puis Kinshasa, en redescendant le fleuve Congo. Une partie de la production de haricot est destinée à l’export pour des marchés spécialisés, comme celle d’Ethiopie pour l’Europe et le Proche-Orient, et celle du nord du la Tanzanie aussi pour l’Europe.
Propriétés
La composition type du haricot commun, par 100 g de partie comestible, est : eau 11,3 g, énergie 1218 kJ (291 kcal), protéines 21,4 g, lipides 1,6 g, glucides 49,7 g, fibres alimentaires 22,9 g, Ca 180 mg, Mg 180 mg, 310 mg, Fe 6,7 mg, Zn 2,8 mg, traces de carotène, thiamine 0,45 mg, riboflavine 0,13 mg, niacine 2,5 mg, vitamine B6 0,56 mg, et traces d’acide ascorbique (Holland, Unwin & Buss, 1991). La composition en acides aminés essentiels, par 100 g de partie comestible, est : tryptophane 210 mg, lysine 1540 mg, méthionine 240 mg, phénylalanine 1130 mg, thréonine 860 mg, valide 990 mg, leucine 1640 mg et isoleucine 890 mg (Paul, Southgate & Russell, 1980). Le haricot est déficient pour certains acides aminés essentiels, comme la méthionine et la cystine. La composition n’est pas en soi un indicateur fiable de la valeur nutritive, car le haricot est peu digeste. Une bonne part du phosphore est liée à des phytates et les protéines ne sont digestibles qu’à 55–65%. Le haricot nécessite généralement une cuisson longue et il peut s’avérer “dur à cuire”, propriété qu’on peut attribuer à des facteurs génétiques et écologiques. Il contient des composés antinutritionnels tels que des lectines (hémagglutinines) et des inhibiteurs de trypsine, mais ils sont inactivés par une cuisson appropriée. Il contient également des tanins et des composés qui provoquent des flatulences.
Son amidon s’est avéré efficace dans la réduction du cholestérol chez le rat, la lectine quant à elle ayant montré une action inhibitrice in vitro contre la transcriptase inverse du VIH-1. Une décoction de gousses a montré des effets hypoglycémiques chez les lapins. Les substances contenues dans le tégument (extraits au méthanol, fractions de tanins et flavonoïdes purs) ont manifesté une activité antioxydante.
Description
- Plante herbacée annuelle, rampante, grimpante, ou érigée et buissonnante, légèrement pubescente ; racine pivotante bien développée, à racines latérales et adventives nombreuses ; tige atteignant 3 m de long, anguleuse ou presque cylindrique.
- Feuilles alternes, 3-foliolées ; stipules triangulaires, petites ; pétiole atteignant 15(–30) cm de long, cannelé sur le dessus, distinctement épaissi à la base, rachis de (1,5–)2,5–3,5(–6) cm de long ; stipelles petites ; folioles ovales, de (5–)7,5–14(–20) cm × 5–10(–15) cm, les latérales asymétriques, la centrale symétrique, entières, légèrement pubescentes, à 3 nervures partant de la base.
- Inflorescence : fausse grappe axillaire ou terminale atteignant 15(–35) cm de long, à fleurs disposées en paires le long du rachis ou solitaires.
- Fleurs bisexuées, papilionacées ; pédicelle atteignant 1 cm de long, mince, à bractéoles ovales ; calice campanulé, tube d’environ 3 mm de long, lobes triangulaires, de 2–3 mm de long ; corolle blanche à violet pâle ou rouge-violet, étendard très largement obovale, cucullé, de 1–1,5 cm de long, ailes obovales, d’environ 2 cm de long, carène brusquement retournée, d’environ 1 cm de long ; étamines 10, dont 9 soudées et 1 libre ; ovaire supère, d’environ 0,5 cm de long, comprimé latéralement, style retourné et en forme de spirale, garni d’un collet de poils fins sous le stigmate ellipsoïde.
- Fruit : gousse linéaire atteignant 20 cm de long, droite ou plus généralement courbe, à bec proéminent, charnue lorsqu’elle est immature, verte ou jaune, parfois rouge, violette ou à zébrures violacées, contenant (2–)5–7(–12) graines.
- Graines globuleuses à réniformes, ellipsoïdes ou oblongues, de 0,5–1,5(–2) cm de long, noires, brunes, jaunes, rouges ou blanches, parfois à motifs marbrés, panachés ou en forme de selle ; hile oblong à elliptique.
- Plantule à germination épigée ; cotylédons oblongs, épais ; deux premières feuilles simples et opposées, feuilles suivantes alternes, 3-foliolées.
Autres données botaniques
Le genre Phaseolus comprend une cinquantaine d’espèces, la plupart se trouvant dans les Amériques. Phaseolus vulgaris est étroitement apparenté à d’autres espèces de Phaseolus, comme Phaseolus coccineus L. (haricot d’Espagne) et Phaseolus acutifolius A.Gray (haricot tépari), assez pour permettre l’hybridation interspécifique.
Les types andins de Phaseolus vulgaris tendent à avoir des graines et des feuilles plus grandes que ceux d’Amérique centrale. Dans chaque pool génique on trouve les différents ports de la plante, mais les types nains déterminés et les types grimpants sont plus courants dans le pool andin que dans le pool d’Amérique centrale. En Afrique tropicale, il existe une certaine diversité génétique que l’on ne trouve pas dans les Amériques.
Les types nains érigés sont plus répandus dans les endroits où l’on pratique la récolte mécanisée, mais aussi dans les petites exploitations. Les types à rames sont limités pour la plupart aux régions de haute altitude, en particulier au sud-ouest de l’Ouganda, au Rwanda, au Burundi et dans les régions orientales de la R.D. du Congo, mais ils sont également cultivés au nord et à l’ouest du Malawi, au nord et au sud de la Tanzanie et au nord de la Zambie. Les types rampants ou semi-grimpants indéterminés, courants dans la plupart des régions de culture du haricot, prédominent dans des conditions de croissance marginales du fait de températures élevées, d’un manque d’eau ou d’une fertilité du sol faible.
Les cultivars à grosses graines rouges marbrées sont très courants en Afrique tropicale, suivis par les cultivars à graines de couleur rouge et de taille petite à moyenne. Les autres types de graines pourraient représenter 50% de la production. Les cultivars à graines noires ou blanches, quant à eux, ne sont pas appréciés en raison de la couleur qu’ils donnent aux plats.
Croissance et développement
Pour permettre la germination du haricot, la température du sol doit être supérieure à 12°C, la levée optimale se situant à des températures du sol de 22–30°C. Les ports des plantes se regroupent grosso-modo en types déterminés ou indéterminés et en types nains ou à rames. Chez le haricot, la floraison débute généralement 28–45 jours après le semis. L’autofécondation est la règle, mais il y a 1–3% d’allofécondation. Les haricots verts peuvent se récolter 25–30 jours après la floraison. Le remplissage des graines peut prendre 23–50 jours. La durée du cycle cultural varie de 60–90 jours pour les types déterminés, et peut atteindre 250–300 jours pour les types indéterminés grimpants. Plusieurs espèces de Rhizobium fixent l’azote avec Phaseolus vulgaris, dont Rhizobium leguminosarum bv. phaseoli, Rhizobium etli et Rhizobium tropici. On considère souvent que le pouvoir de fixation de l’azote du haricot est moins bon que celui d’autres légumes secs comme le niébé, le soja et l’arachide, mais on a quand même noté des taux de fixation atteignant 125 kg d’azote par ha.
Ecologie
En Afrique tropicale, le haricot est bien adapté à des altitudes de 1200–2200 m, où les températures moyennes pendant la saison de croissance sont de 15–23°C. Il n’empêche que 20% de la production de haricot en Afrique tropicale se fait à une température moyenne supérieure à 23°C. La plante supporte de temps en temps des températures journalières de 35°C, mais cela aboutit souvent à l’avortement des fleurs. La croissance s’arrête en dessous de 10°C et le gel tue la plante. A des latitudes supérieures à 10°, Phaseolus vulgaris peut se cultiver à basse altitude au cours des mois les plus frais, en général sous irrigation et d’habitude pour une récolte de haricots verts. On trouve des productions de haricot là où la pluviométrie moyenne au cours de la saison de croissance est de 250 mm ; toutefois on estime que 65% de la production a lieu dans les régions où la moyenne pluviométrique est supérieure à 400 mm en saison. Des déficits en eau temporaires réduisent sérieusement les rendements. Mais plus graves encore que le manque d’eau sont les maladies favorisées par un temps humide. Les génotypes du haricot commun diffèrent en matière de sensibilité à la photopériode (plantes de jours courts ou indifférentes) ; cette sensibilité est d’ordinaire plus grande chez les génotypes d’origine andine que chez les méso-américains.
Les sols à texture moyenne et bien drainés de plus de 0,5 m de profondeur ont la préférence du haricot, qui est sensible à l’acidité du sol, y compris les toxicités à l’aluminium et au manganèse qui lui sont associées. Le pH optimal est de 6,0–7,5, mais en Afrique tropicale la majeure partie de la production se fait sur des sols dont le pH est de 5–6, et pour 20% elle a lieu sur des sols à pH inférieur à 5. En Afrique tropicale, la production de haricot se fait surtout dans des conditions de carence en phosphore. Là où des espèces de Phaseolus n’ont pas été cultivées auparavant, la fixation d’azote par symbiose peut ne pas suffire à satisfaire les besoins de la plante en azote.
Multiplication et plantation
Le haricot se multiplie habituellement par graines, mais la multiplication végétative par boutures est possible. Le poids de 1000 graines est de 150–600 g. Le haricot peut se semer à la volée et en lignes. En culture pure, les densités de semis sont de 150 000–400 000 graines à l’ha. En culture associée, elles sont moins élevées. Le haricot à port grimpant indéterminé se sème à raison de 3–6 graines par trou de plantation sur des lignes espacées de 100–120 cm, en ménageant des espaces sur la ligne de 40–50 cm. On enfouit généralement les graines à 3–4 cm de profondeur, mais on peut aller jusqu’à 7 cm si la surface du sol est sèche et pas trop lourde ni trop sujette à l’encroûtement. Il est courant d’employer des mélanges de plusieurs types de semences, comme au Rwanda, en Tanzanie et au Malawi. Dans l’agriculture traditionnelle, la terre se prépare à la main ou à l’aide d’animaux de labour avant le semis. La culture se pratique surtout en terrain plat, mais cela n’exclut pas le recours à des buttes ou des billons lorsque le sol est lourd ou la nappe phréatique élevée. 30% seulement de la superficie de production de haricot en Afrique tropicale est cultivé en culture pure. Les associations avec le maïs, le bananier et les plantes à racines ou à tubercules sont fréquentes, représentant respectivement 40–50%, 10–20% et 10–20% de la superficie cultivée en haricot commun. Moins fréquentes sont les associations avec le sorgho, le mil, les pois, les fèves, le caféier et d’autres espèces. Les cultivars grimpants sont plus souvent produits en culture pure que les types non grimpants, mais la densité de leur feuillage crée un environnement humide, qui favorise les maladies. Le haricot est parfois cultivé comme culture de relais, profitant de l’humidité résiduelle, par ex. au Malawi et dans le sud de la Tanzanie.
Gestion
Pour les cultivars grimpants, des rames de 2 m (en général des branches droites ou des tiges de bambou, ou encore de Pennisetum) sont placées après la levée pour soutenir les plantes. On ne désherbe qu’une ou deux fois, et après cela le couvert végétal est suffisamment développé pour étouffer les adventices. Le buttage s’effectue souvent environ 3 semaines après le semis. Cette tâche demande du soin car le collet du haricot est facilement endommagé. L’irrigation n’est pas souvent pratiquée, sauf à des latitudes élevées, où la production a lieu en hiver (la saison sèche). On a rarement recours à des engrais en Afrique tropicale, même si les carences en N et en P constituent des contraintes importantes. Des apports adéquats en P sont décisifs pour la fixation symbiotique de l’azote et il y a souvent une réaction économique à 20 kg de N et 22 kg de P par ha. Bien que dans l’ensemble le haricot soit produit sur des sols acides, le recours à une correction avec de la chaux n’est pas courant. La rotation avec d’autres espèces annuelles ou vivaces à vie courte est pratiquée ; le plus souvent avec des céréales, d’autres légumes secs ou des plantes à racines ou à tubercules.
Maladies et ravageurs
Le haricot commun est extrêmement sensible aux maladies et aux ravageurs et on estime que plus de 50% de la production est perdue chaque année en Afrique tropicale. Les maladies fongiques transmises par les graines, comme les taches anguleuses des feuilles (Phaeoisariopsis griseola) et l’anthracnose (Colletotrichum lindemuthianum), ainsi que les maladies bactériennes comme le flétrissement (Xanthomonas campestris pv. phaseoli) et la graisse à halo (Pseudomonas savastanoi pv. phaseolicola, synonyme : Pseudomonas syringae pv. phaseolicola) font partie des contraintes principales qui pèsent sur la production de haricot. Les pertes de rendements attribuées à ces maladies sont évaluées à plus de 1 million t par an en Afrique subsaharienne. La maladie des taches anguleuses et l’anthracnose sont sensibles à de nombreux fongicides, mais il est rare que les petits paysans emploient des produits chimiques pour lutter contre les maladies. Les cultivars varient dans leur réaction à ces maladies. La fonte des semis en pré- et post-levée, provoquée par des complexes de pourriture des racines (Pythium aphanidermatum, Rhizoctonia solani (groupe AG4) et Fusarium solani f.sp. phaseoli), a un gros impact dans les régions où la production du haricot est intensive et la fertilité du sol peu élevée. Améliorer l’apport en nutriments et utiliser des cultivars résistants ou tolérants sont des méthodes efficaces pour réduire les pertes dues à cette pourriture des racines. D’après les estimations, le virus de la mosaïque commune du haricot (BCMV), transmis par les pucerons et les graines, serait responsable de 180 000 t de pertes de rendement par an en Afrique subsaharienne. La résistance au BCMV est le fait d’un gène dominant unique, mais c’est ce même gène qui est la cause d’une sensibilité au virus de la mosaïque nécrotique commune du haricot (BCMNV, également connu sous le nom de “racine noire”), indigène à l’Afrique. Ces virus étroitement apparentés possèdent chacun plus d’un groupe de pathogénicité. La résistance à la totalité des groupes peut être obtenue en déployant au moins 2 gènes récessifs. N’utiliser que des semences exemptes de maladies peut être utile pour lutter contre les maladies transmises par les graines, mais de telles semences sont rares. La rouille commune du haricot (Uromyces appendiculatus), l’ascochytose (Phoma exigua), l’oïdium (Erysiphe polygoni) et le rhizoctone (Rhizoctonia solani groupe AG1) peuvent entraîner conjointement des pertes de rendement de 600 000 t/an en Afrique subsaharienne.
Les insectes ravageurs les plus importants sont les mouches mineuses du haricot (Ophiomyia spp.), surtout aux stades de croissance initiaux et lorsque les plantes subissent un stress du fait de carences en eau et en nutriments. On peut lutter contre les mouches du haricot en traitant les semences avec un insecticide systémique, tel que l’imidaclopride ou l’endosulphan, soit en traitement des semences elles-mêmes, soit en pulvérisation peu après la levée. En Afrique, les vers gris (Agrotis spp.) et les chenilles (Spodoptera spp.) peuvent poser problème, en particulier sur les sols corrigés au fumier de ferme, pratique répandue chez les petits paysans. Les thrips (Frankliniella occidentalis, Frankliniella schultzei et Megalurothrips sjostedti) sont à l’origine de 80 000–90 000 t de pertes de rendement par an et les insectes foreurs des gousses (Helicoverpa armigera, Maruca testulalis et Clavigralla spp.) de 130 000–140 000 t en Afrique subsaharienne. Il est difficile de lutter contre les thrips, en particulier Frankliniella occidentalis, car ils sont résistants à de nombreux pesticides couramment utilisés. On peut facilement venir à bout des foreurs de gousses à l’aide de produits à base de Bacillus thuringiensis. Les pucerons (Aphis fabae et Aphis craccivora) figurent parmi les 10 principales contraintes de la production de haricot et c’est pire lorsqu’il fait sec. La chrysomèle Ootheca provoque des dégâts un peu partout en Afrique subsaharienne. L’aleurode (Bemisia tabaci), un charançon cigarier malgache (Apoderus humeralis) et la belle-dame (Vanessa cardui, synonyme : Pyrameis cardui) n’ont d’importance que localement. Les bruches (Zabrotes subfasciatus et Acanthoscelides obtectus) sont les ravageurs principaux du haricot stocké ; elles viendraient en sixième place parmi les causes principales de pertes de rendement (250 000 t/an) en Afrique subsaharienne. La lutte contre les ravageurs, comme toujours, fait intervenir la mise en œuvre conjointe de plusieurs pratiques à faible coût, dont la rotation des cultures, les cultures associées, le semis de cultivars résistants ou tolérants, et le recours aux insecticides.
Récolte
Le haricot peut se récolter lorsque la plupart des gousses sont encore vertes mais proches de leur maturité physiologique, afin d’avoir une récolte précoce d’un légume sec frais et facile à cuire ; toutefois, la plupart des cultures se récoltent à maturité. En Afrique tropicale, la récolte s’effectue presque entièrement à la main. Les plantes des haricots non grimpants s’arrachent d’habitude lorsque la plupart des gousses sont sèches, puis on les met en bottes et on les rentre. Les gousses des types grimpants se récoltent généralement à la main au fur et à mesure qu’elles mûrissent, et la récolte s’échelonne ainsi sur plusieurs semaines.
Rendements
Le rendement moyen du haricot est d’environ 1,5 t/ha en Europe et dans les pays industrialisés d’Asie, de 1 t/ha en Amérique du Nord et de 0,7 t/ha au niveau mondial. En Afrique tropicale, cette moyenne tourne en général autour de 0,6 t/ha. Lorsque les meilleures conditions possibles sont réunies, on peut atteindre des rendements de 2,5 t/ha pour les types non grimpants et de 5 t/ha pour les types grimpants. Sous irrigation, au Malawi par exemple, des rendements de 3,8 t/ha ont été obtenus.
Traitement après récolte
Les petits paysans rapportent les haricots récoltés chez eux pour les étaler au sol et les faire sécher au soleil. Après séchage, le battage s’effectue soit avec de longs bâtons, soit avec un tracteur que l’on fait passer sur la récolte mise en tas, ou plus rarement, avec une batteuse mécanique. Avant d’être stockées, les graines de haricot sont souvent séchées au soleil afin de détruire les bruches et de diminuer le taux d’humidité, ce qui permet une meilleure conservation. Mais un séchage prolongé peut entraîner une difficulté de cuisson. Dans certaines régions, les graines sont triées par type, tandis qu’ailleurs, ce sont des mélanges complexes qui sont intentionnellement produits et consommés. La conservation des graines se fait avec de la cendre de bois, des feuilles de tabac ou de la cendre de tiges de haricot.
Ressources génétiques
Le haricot est menacé d’érosion génétique en raison de pratiques agricoles non traditionnelles où un nombre relativement restreint de génotypes sont produits en peuplements purs, et, surtout en Amérique Latine, à cause du remplacement de cette culture par d’autres plus rentables. Une conservation in situ peut être intéressante, surtout pour des pays comme le Rwanda où l’on trouve de nombreuses variétés traditionnelles cultivées dans des conditions diverses, souvent en mélanges complexes qui regroupent jusqu’à 20 types de graines différentes.
La plus vaste collection ex situ de Phaseolus se trouve au Centre international d’agriculture tropicale (CIAT) près de Cali (Colombie). Elle contient plus de 40 000 entrées, sur lesquelles 35 000 sont des Phaseolus vulgaris. D’après les estimations, cette collection représenterait 50–75% de la variabilité présente dans les centres de diversification pour les types domestiqués, mais seulement moins de 30% de la diversité des types sauvages. Parmi les collections de ressources génétiques détenues en Afrique, citons : Bunda Agricultural College de Lilongwe, au Malawi (6000 entrées), National Genebank of Kenya, KARI, de Kikuyu (3000 entrées) et l’Institut des sciences agronomiques du Rwanda, à Butare (3000 entrées). Les programmes d’amélioration génétique nationaux en Afrique (comme celui d’Ouganda) possèdent des collections de variétés locales plus petites.
Sélection
En Afrique et dans les autres pays du monde, les programmes d’amélioration génétique du haricot ont pour but d’améliorer le potentiel de rendement ; une bonne partie des progrès réalisés porte sur l’amélioration de la tolérance ou de la résistance aux contraintes biotiques et abiotiques. Améliorer la résistance aux maladies est l’objectif principal des sélectionneurs, et des réussites importantes ont été obtenues ; cependant, il est fréquent que la résistance ne soit pas durable en raison de la diversité génétique des agents pathogènes et de leur aptitude à s’adapter. La résistance au flétrissement bactérien commun a été introduite à partir de Phaseolus coccineus et de Phaseolus acutifolius. Une meilleure résistance aux insectes est un autre objectif d’amélioration important. Les espèces sauvages de Phaseolus ont été une source utile de gènes, comme pour la résistance à la bruche Zabrotes subfasciatus. Les sélections visant à obtenir une tolérance aux stress abiotiques ont gagné en importance et, en Afrique, des lignées dotées d’une tolérance supérieure aux sols acides, ainsi que d’autres capables d’utiliser efficacement N ou P, ont été mises sur le marché. Les progrès en matière de tolérance à la sécheresse sont prometteurs : à la profondeur des systèmes racinaires a été associée une efficacité dans l’acheminement des glucides depuis les feuilles jusqu’aux graines lorsque la plante subit un stress dû à la sécheresse. La descendance produite à partir de croisements entre les pools géniques andin et méso-américain est habituellement faible et peu productive, mais les sélectionneurs ont mis au point des lignées et des géniteurs supérieurs au moyen de croisements inter-pools qui combinent les caractères supérieurs de chacun des pools.
En Afrique, des programmes d’amélioration limités en ressources ont profité d’une collaboration tant au niveau régional qu’international, par exemple du matériel génétique élaboré au CIAT.
L’amélioration génétique du haricot gagne en efficacité grâce au recours de plus en plus fréquent aux marqueurs moléculaires. L’initiative “Phaseomics” facilite la collaboration entre instituts de recherche pour mettre sur pied une bibliothèque d’ADNc et séquencer le génome du haricot. La régénération in vitro du haricot à des fins d’amélioration génétique est possible à l’aide de différents explants : méristèmes apicaux, pétioles, plantules, axes d’embryon, cotylédons, nœuds de plantules et cals méristématiques. On n’a jamais confirmé l’existence de plantes de haricot transgéniques stables à partir de systèmes d’Agrobacterium tumefaciens, mais des plantes transgéniques ont été obtenues par bombardement de particules. Toutefois, la manière la plus efficace d’améliorer le haricot par transgenèse est sans doute d’utiliser Phaseolus acutifolius, que l’on peut transformer en routine à l’aide d’Agrobacterium, puis de croiser les plantes transgéniques ainsi obtenues avec le haricot commun à l’aide de la technique de sauvetage d’embryons.
Perspectives
Le haricot commun est le légume sec le plus consommé au monde ; en Afrique tropicale, c’est une espèce cultivée importante, en particulier en Afrique centrale, orientale et australe, aussi bien pour sa valeur nutritionnelle que pour son potentiel commercial. Il a surtout de l’importance pour les petits paysans et les femmes, qui sont souvent responsables de sa culture. Le commerce régional pèse un certain poids économique dans quelques pays, et il existe aussi en Afrique tropicale une production de haricot destinée à l’export vers l’Europe et le Proche-Orient. Il n’y a pas de raison de croire qu’à l’avenir l’importance du haricot va diminuer ; en Afrique tropicale, il est même probable que la demande augmentera en même temps que la population. La production de haricot en Afrique tropicale est limitée par sa sensibilité aux maladies et aux ravageurs. En dépit des progrès considérables réalisés dans l’amélioration génétique en vue de la résistance ou de la tolérance aux maladies et aux ravageurs, des travaux restent à accomplir, car la résistance n’est souvent pas durable. Une sélection pour une meilleure tolérance à des stress abiotiques tels que la toxicité de l’aluminium, et pour une utilisation plus efficace par la plante de l’eau et des nutriments du sol, est également nécessaire afin d’accroître la production tant sur les sols marginaux que sur les sols productifs. Les outils biotechnologiques vont jouer un rôle de plus en plus grand dans la sélection du haricot, par ex. le recours à la cartographie moléculaire pour localiser les gènes de résistance.
Références principales
- Abate, T. & Ampofo, J.K.O., 1996. Insect pests of beans in Africa: their ecology and management. Annual Review of Entomology 41: 45–73.
- Allen, D.J., Buruchara, R.A. & Smithson, J.B., 1998. Diseases of common bean. In: Allen, D.J. & Lenné, J.M. (Editors). The pathology of food and pasture legumes. CAB International, Wallingford, United Kingdom. pp. 179–265.
- Baudoin, J.P., Vanderborght, T., Kimani, P.M. & Mwang’ombe, A.W., 2001. Common bean. In: Raemaekers, R.H. (Editor). Crop production in tropical Africa. DGIC (Directorate General for International Co-operation), Ministry of Foreign Affairs, External Trade and International Co-operation, Brussels, Belgium. pp. 317–326.
- Gepts, P. & Debouck, D., 1991. Origin, domestication, and evolution of the common bean. In: van Schoonhoven, A. & Voysest, O. (Editors). Common beans: research for improvement. CIAT, Cali, Colombia and CAB International, Wallingford, United Kingdom. pp. 7–54.
- Hidalgo, R., 1991. CIAT’s world Phaseolus collection. In: van Schoonhoven, A. & Voysest, O. (Editors). Common beans: research for improvement. CIAT, Cali, Colombia and CAB International, Wallingford, United Kingdom. pp. 163–198.
- Messiaen, C.-M. & Seif, A.A., 2004. Phaseolus vulgaris L. (French bean). In: Grubben, G.H.J. & Denton, O.A. (Editors). Plant Resources of Tropical Africa 2. Vegetables. PROTA Foundation, Wageningen, Netherlands / Backhuys Publishers, Leiden, Netherlands / CTA, Wageningen, Netherlands. pp. 415–419.
- Popelka, J.C., Terryn, N. & Higgins, T.J.V., 2004. Gene technology for grain legumes: can it contribute to the food challenge in developing countries? Plant Science 167: 195–206.
- Shellie-Dessert, K.C. & Bliss, F.A., 1991. Genetic improvement of food quality factors. In: van Schoonhoven, A. & Voysest, O. (Editors). Common beans: research for improvement. CIAT, Cali, Colombia and CAB International, Wallingford, United Kingdom. pp. 649–678.
- Smartt, J., 1989. Phaseolus vulgaris L. In: van der Maesen, L.J.G. & Somaatmadja, S. (Editors). Plant Resources of South-East Asia No 1. Pulses. Pudoc, Wageningen, Netherlands. pp. 60–63.
- Wortmann, C.S., Kirkby, R.A., Eledu, C.A. & Allen, D.J., 1998. Atlas of common bean (Phaseolus vulgaris) production in Africa. CIAT Publication 297. CIAT, Cali, Colombia. 133 pp.
Autres références
- Beninger, C.W. & Hosfield, G.L., 2003. Antioxidant activity of extracts, condensed tannin fractions, and pure flavonoids from Phaseolus vulgaris L. seed coat color genotypes. Journal of Agricultural and Food Chemistry 51(27): 7879–7883.
- Chacon, S., M.I., Pickersgill, B. & Debouck, D.G., 2005. Domestication patterns in common bean (Phaseolus vulgaris L.) and the origin of the Mesoamerican and Andean cultivated races. Theoretical and Applied Genetics 110(3): 432–444.
- Debouck, D.G. & Smartt, J., 1995. Beans. In: Smartt, J. & Simmonds, N.W. (Editors). Evolution of crop plants. 2nd Edition. Longman, London, United Kingdom. pp. 287–294.
- Freytag, G. & Debouck, D.G., 2002. Taxonomy, distribution and ecology of the genus Phaseolus (Leguminosae - Papilionoideae) in North America, Mexico and Central America. Botanical Institute of Texas, Fort Worth, Texas, United States. 300 pp.
- Fukushima, M., Ohashi, T., Kojima, M., Ohba, K., Shimizu, H., Sonoyama, K. & Nakano, M., 2001. Low density lipoprotein receptor mRNA in rat liver is affected by resistant starch of beans. Lipids 36(2): 129–134.
- Giller, K.E., 2001. Nitrogen fixation in tropical cropping systems. 2nd Edition. CAB International, Wallingford, United Kingdom. 423 pp.
- Gillett, J.B., Polhill, R.M., Verdcourt, B., Schubert, B.G., Milne-Redhead, E., & Brummitt, R.K., 1971. Leguminosae (Parts 3–4), subfamily Papilionoideae (1–2). In: Milne-Redhead, E. & Polhill, R.M. (Editors). Flora of Tropical East Africa. Crown Agents for Oversea Governments and Administrations, London, United Kingdom. 1108 pp.
- Graham, P.H. & Ranalli, P., 1997. Common bean (Phaseolus vulgaris L.). Field Crops Research 53: 131–146.
- Hanelt, P. & Institute of Plant Genetics and Crop Plant Research (Editors), 2001. Mansfeld’s encyclopedia of agricultural and horticultural crops (except ornamentals). 1st English edition. Springer Verlag, Berlin, Germany. 3645 pp.
- Hidalgo, R. & Beebe, S., 1997. Phaseolus beans. In: Fuccillo, D., Sears, L. & Stapleton, P. (Editors). Biodiversity in trust: conservation and use of plant genetic resources in CGIAR centres. Cambridge University Press, Cambridge, United Kingdom. pp. 139–155.
- Holland, B., Unwin, I.D. & Buss, D.H., 1991. Vegetables, herbs and spices. The fifth supplement to McCance & Widdowson’s The Composition of Foods. 4th Edition. Royal Society of Chemistry, Cambridge, United Kingdom. 163 pp.
- Johnson, N.L., Pachico, D. & Wortmann, C.S., 2003. The impact of CIAT’s genetic improvement research on beans. In: Evenson, R.E. & Gollin, D. (Editors). Crop variety improvement and its effect on productivity: the impact of international agricultural research. CABI Publishing, Wallingford, United Kingdom. pp. 257–274.
- Kay, D.E., 1979. Food legumes. Crops and Product Digest No 3. Tropical Products Institute, London, United Kingdom. 435 pp.
- Mackinder, B., Pasquet, R., Polhill, R. & Verdcourt, B., 2001. Leguminosae (Papilionoideae: Phaseoleae). In: Pope, G.V. & Polhill, R.M. (Editors). Flora Zambesiaca. Volume 3, part 5. Royal Botanic Gardens, Kew, Richmond, United Kingdom. 261 pp.
- Martínez Romero, E., 2003. Diversity of Rhizobium - Phaseolus vulgaris symbiosis: overview and perspectives. Plant and Soil 252: 11–23.
- Paul, A.A., Southgate, D.A.T. & Russell, J., 1980. First supplement to McCance and Widdowson’s The composition of foods: amino acids (mg per 100 g food), fatty acids (g per 100 g food). Elsevier, Amsterdam, Netherlands. 112 pp.
- Qi, A., Smithson, J.B. & Summerfield, R.J., 1998. Adaptation to climate in common bean (Phaseolus vulgaris L.): photothermal flowering responses in the eastern, southern and Great Lakes regions of Africa. Experimental Agriculture 34(2): 153–170.
- Roman-Ramos, R., Flores-Saenz, J.L. & Alarcon-Aguilar, F.J., 1995. Anti-hyperglycemic effect of some edible plants. Journal of Ethnopharmacology 48: 25–32.
- Wang, H.X. & Ng, T.B., 2000. Examination of lectins, polysaccharopeptide, alkaloid, coumarin and trypsin inhibitors for inhibitory activity against Human Immunodeficiency Virus reverse transcriptase and glycohydrolases. Planta Medica 67(7): 669–672.
- Westphal, E., 1974. Pulses in Ethiopia, their taxonomy and agricultural significance. Agricultural Research Reports 815. Centre for Agricultural Publishing and Documentation, Wageningen, Netherlands. 263 pp.
Sources de l’illustration
- Smartt, J., 1989. Phaseolus vulgaris L. In: van der Maesen, L.J.G. & Somaatmadja, S. (Editors). Plant Resources of South-East Asia No 1. Pulses. Pudoc, Wageningen, Netherlands. pp. 60–63.
Auteur(s)
- C.S. Wortmann, Department of Agronomy and Horticulture, University of Nebraska Lincoln, IANR, 154 Keim Hall, Lincoln, NE 68583–0915, United States
Citation correcte de cet article
Wortmann, C.S., 2006. Phaseolus vulgaris L. - haricot sec. In: Brink, M. & Belay, G. (Editeurs). PROTA 1: Cereals and pulses/Céréales et légumes secs. PROTA, Wageningen, Pays Bas. Consulté le 19 décembre 2024.
- Voir cette page sur la base de données Prota4U