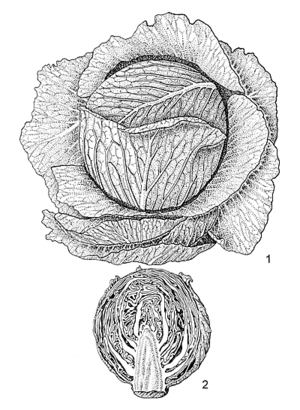
Brassica oleracea - chou pommé (PROTA)
Introduction |
| Importance générale | |
| Répartition en Afrique | |
| Répartition mondiale | |
| Légume | |
| Fourrage | |
| Sécurité alimentaire | |
Brassica oleracea L. (chou pommé)
- Protologue : Sp. pl. 2: 667 (1753).
- Famille : Brassicaceae (Cruciferae)
- Nombre de chromosomes : 2n = 18
Noms vernaculaires
- Chou pommé, chou cabus (Fr).
- Headed cabbage, cabbage (En).
- Couve repolho (Po).
- Kabichi, kabichu (Sw).
Origine et répartition géographique
Le chou pommé a évolué dans le nord-ouest de l’Europe au début du Moyen-Age à partir de choux verts non ramifiés à tige mince introduits à l’époque romaine depuis la région méditerranéenne, où Brassica oleracea et les espèces apparentées existent à l’état naturel dans les zones côtières. Il est possible que les types sauvages de Brassica oleracea poussant sur les côtes d’Europe occidentale aient contribué à cette évolution. Alors que les types primitifs étaient cultivés à l’origine à des fins médicinales, le chou pommé est devenu un des légumes les plus importants de l’Europe du XVIe siècle. A partir de cette époque, le chou pommé a été introduit dans le monde entier. Dans les régions tropicales et subtropicales, la culture commerciale reste cantonnée aux climats frais des hautes terres ou aux saisons fraîches sous les latitudes plus élevées. En Afrique, le chou pommé est surtout commun en Afrique de l’Est et en Egypte.
Usages
Le chou pommé se consomme généralement comme légume cuit (à l’eau ou à l’huile), parfois confit. Il se mange également cru en salade, une fois coupée en lanières ou haché (“coleslaw” en anglais), ou en salade mixte. On peut le conserver après étuvage et séchage, ou bien par fermentation anaérobie dans la saumure (choucroute).
Production et commerce international
Au cours des dernières décennies, le chou pommé a pris de plus en plus d’importance dans les régions tropicales et subtropicales, en particulier le chou blanc précoce à pomme ferme et de forme ronde à plate (1–2,5 kg). Il peut être produit assez facilement en grandes quantités, transporté sur de grandes distances sans s’abîmer et se conserver pendant quelques semaines. Les cultures de chou pommé représentent une superficie estimée en 2002 à environ 3 millions d’ha dans 124 pays (la production avoisine les 62,5 millions de t), répartie comme suit : 2 millions d’ha en Asie (dont 1,5 million d’ha en Chine), 0,5 million d’ha en Europe, 180 000 ha dans les deux Amériques, et l’équivalent de 100 000 ha en Afrique. Il n’y a pas de données annuelles fiables sur les superficies cultivées de chou pommé pour la plupart des pays d’Afrique tropicale. Si l’on se base sur les ventes de semences commerciales, au moins 40 000 ha de chou pommé sont cultivés dans la région formée par le Kenya, l’Ouganda et la Tanzanie, 10 000 ha dans la région comprenant le Malawi, la Zambie et le Zimbabwe, 4000 ha en Ethiopie et 3000 ha au Cameroun. Presque toute la production de chou blanc est destinée aux marchés locaux urbains. Le Mozambique importe des quantités considérables de chou pommé d’Afrique du Sud, et faisait de même du Zimbabwe jusqu’à une époque récente.
Propriétés
La composition nutritionnelle du chou blanc par 100 g de partie comestible (c.à.d. 77% du produit tel qu’acheté) est de : eau 90,1 g, énergie 109 kJ (26 kcal), protéines 1,7 g, lipides 0,4 g, glucides 4,1 g, fibres alimentaires 2,9 g, Ca 52 mg, Mg 8 mg, P 41 mg, Fe 0,7 mg, Zn 0,3 mg, carotène 385 μg, thiamine 0,15 mg, riboflavine 0,02 mg, niacine 0,5 mg, folate 75 μg, acide ascorbique 49 mg (Holland, B., Unwin, I.D. & Buss, D.H., 1991).
Tous les Brassica contiennent des glucosinolates qui, dans les feuilles broyées, sont hydrolysés par l’enzyme myrosinase essentiellement en thiocyanates de goût amer et en isothiocyanates volatiles ; ces composants ont des propriétés antimicrobiennes et anticarcinogènes. Dans le chou pommé, la teneur en glucosinolates est relativement faible (100 mg par 100 g), ce qui résulte de siècles de sélection pour éliminer les plantes de goût amer. Malgré sa longue histoire, le chou pommé n’a apparemment aucune application médicinale.
Description
- Plante herbacée bisannuelle, érigée, glabre, atteignant 60 cm de haut lors de sa maturité végétative, et 200 cm au moment de la floraison, à tige non ramifiée atteignant 30 cm de long, s’épaississant progressivement vers le haut ; système racinaire fortement ramifié.
- Feuilles alternes mais serrées les unes contre les autres, sessiles, feuilles basales formant une rosette, feuilles supérieures rassemblées en une pomme compacte globuleuse aplatie à ellipsoïde, atteignant 30 cm de diamètre, généralement simples ; stipules absentes ; limbe ovale à obovale ou quasi-circulaire, atteignant 35 cm × 30 cm, ondulé ou incisé de façon irrégulière à presque entier, couvert d’une couche cireuse, blanchâtre à vert pâle à nervures blanchâtres (chou blanc), rouge-violet (chou rouge), ou vert à jaune-vert et frisé (chou de Milan).
- Inflorescence : grappe terminale paniculée atteignant 100 cm de long.
- Fleurs bisexuées, régulières, 4-mères ; pédicelle atteignant 2 cm de long, ascendant ; sépales oblongs d’environ 1 cm de long, érigés ; pétales obovales, de 1,5–2,5 cm de long, à onglet, jaune pâle à jaune vif ou blanchâtres ; étamines 6 ; ovaire supère, cylindrique, 2-loculaire, stigmate globuleux.
- Fruit : silique linéaire de 5–10 cm × 5 mm environ, pourvue d’un bec effilé de 5–15 mm de long, déhiscente, contenant jusqu’à 30 graines.
- Graines globuleuses, de 2–4 mm de diamètre, finement réticulées, brunes.
- Plantule à germination épigée, développant une racine pivotante et des racines latérales ; hypocotyle de 3–5 cm de long, épicotyle absent ; cotylédons à pétiole de 1–2 cm de long, limbe cordé, de 1–1,5 cm de long, cunéiforme à la base, émarginé à l’apex.
Autres données botaniques
Le chou pommé a été classé dans la convar. capitata (L.) Alef., subdivisée en var. capitata L. qui comprend le chou blanc (à feuilles lisses, blanches à vertes) et le chou rouge (à feuilles rouges), et la var. sabauda L. qui comprend le chou de Milan (à feuilles vertes frisées). Il vaut mieux considérer ces 3 types de choux pommés comme des groupes de cultivars, qui sont respectivement le Groupe Chou blanc, le Groupe Chou rouge et le Groupe Chou de Milan. Toutefois, on estime souvent qu’une distinction formelle entre ces groupes au niveau mondial est superflue et porte à confusion, bien qu’elle puisse être pertinente au niveau local.
On cultive des centaines de cultivars de chou pommé dans le monde. Chez les maraîchers des régions tropicales, des hybrides F1 de chou blanc, précoces et à pomme compacte et arrondie ou aplatie, remplacent de plus en plus souvent les variétés -populations telles que ‘Golden Acre’, ‘Copenhagen Market’, ‘Glory of Enkhuizen’, ‘Drumhead’ à pomme aplatie et ‘Sugarloaf’ à pomme pointue (“pain de sucre”). Comme exemples de ces cultivars hybrides F1, on citera : ‘Fresco’, ‘Gloria’ (= ‘Green Boy’), ‘Green Coronet’, ‘KK Cross’, ‘KY Cross’ et ‘Hercules’. Les hybrides de chou blanc d’origine japonaise et taïwanaise en particulier sont souvent précoces et tolérants à la chaleur. Technisem commercialise plusieurs cultivars adaptés aux basses terres tropicales (par ex. les zones côtières voisines de Dakar et d’Abidjan), dont ‘KK Cross’, ‘Fabula’, ‘Rustica’ et ‘Sahel’, qui peuvent être récoltés 60–80 jours après la plantation, ainsi que les très précoces ‘Quick Start’ et ‘Bali’ (45–55 jours), mais dont la pomme est plus petite. Tous ces cultivars sont résistants à Xanthomonas ; ‘Fabula’, ‘Rustica’ et ‘Sahel’ sont également résistants à Fusarium.
Le chou rouge et le chou de Milan sont surtout importants économiquement en Europe et en Amérique, mais ils ne sont pas communs dans les régions tropicales. Comme exemples de cultivar taïwanais de chou rouge, on peut citer ‘Scarlet’ et ‘Sunny Side’. Le cultivar de chou rouge ‘Red Ball’ de Technisem est tolérant à la chaleur et à Xanthomonas.
Croissance et développement
Les graines germent au bout de 3–6 jours et les plantules ont 4 vraies feuilles 4–5 semaines après un semis à des températures quotidiennes moyennes de 15–20°C. Les 7–15 premières feuilles s’ouvrent et se déploient jusqu’à former une rosette de feuilles extérieures, appelée “frame” en anglais. Les feuilles suivantes se développent en calotte et, en se recouvrant, forment l’enveloppe de la pomme ; le bourgeon terminal grossit, la tige s’épaissit et la pomme se remplit de feuilles charnues. La pomme est pleine et prête à être récoltée 80–120 jours après la germination, en fonction du génotype et du climat.
La plupart des types de chou pommé demandent à être exposés à des températures inférieures à 10°C pendant 6–8 semaines pour l’initiation florale et la montaison. La tige principale s’allonge rapidement, ce qui fait éclater la pomme, et évolue en une inflorescence ramifiée. La floraison commence à la base de l’inflorescence, 2–3 mois après les premiers signes de la montaison, et se poursuit pendant 4–5 semaines. Une auto-incompatibilité sporophytique (système à 1 locus à allèles multiples) empêche l’autofécondation naturelle. Ce sont les insectes, en particulier les abeilles, qui effectuent la pollinisation croisée. Les graines sont mûres 8–10 semaines après l’anthèse.
Ecologie
Le chou pommé pousse bien à des températures journalières moyennes de 15–20°C avec une variation diurne d’au moins 5°C. Dans les régions tropicales, ces conditions ne sont remplies que sur les hautes terres, au-dessus de 800 m d’altitude. A des températures supérieures à 25°C, les jeunes plantes se développent encore correctement, mais ensuite la pommaison prend du retard. Certains hybrides F1 japonais et taïwanais sont plus tolérants à la chaleur, mais même eux ne donnent pas de bons résultats dans les conditions des basses terres tropicales.
La plupart des cultivars de chou pommé sont indifférents à la photopériode et ce sont essentiellement les faibles températures qui induisent l’initiation florale. Les plantes en cours de croissance peuvent même supporter de courts épisodes de gel ( –5°C).
Il faut que les sols soient bien drainés et fertiles, qu’ils aient une bonne capacité de rétention d’eau, une forte teneur en matière organique et un pH de 6,5–7,5. En raison de son système racinaire superficiel, le chou pommé nécessite un apport régulier en eau pendant toute sa période de croissance, sous forme de pluie ou d’arrosage. L’évapotranspiration d’un champ de choux pommés à maturité peut atteindre 4 mm par jour.
Multiplication et plantation
Les graines sèches de chou pommé (dont la teneur en humidité est de 6%) restent viables pendant au moins 4–6 ans si elles sont conservées au sec à des températures inférieures à 18°C. Les graines qui viennent d’être récoltées germent parfois mal. Un trempage pendant la nuit et un rinçage à l’eau permettent de surmonter ce problème. Au bout de 3–4 mois de stockage, la dormance est levée. On sème les graines en planches, en pots ou sur des plateaux ; il peut être nécessaire de protéger les jeunes plants contre un ensoleillement trop vif au moyen d’un léger ombrage. Il faut près de 300–500 g de semences et environ 200 m2 de planches de semis pour produire 1 ha de choux. Le poids de 1000 graines est de 3–5 g. Le repiquage en plein champ a lieu 4–5 semaines plus tard, lorsque les plants ont 4–6 vraies feuilles. On observe généralement des densités de plantation de 30 000–50 000 plantes par ha et des espacements de 40–50 cm × 55–60 cm. On peut plus ou moins contrôler la taille des pommes en modulant la densité de plantation.
Les rejets latéraux prélevés sur les trognons décapités peuvent prendre racine et être repiquées. Cette méthode de multiplication végétative est pratiquée dans les programmes de sélection pour maintenir les plantes sélectionnées.
Gestion
Le chou pommé est souvent cultivé en rotation avec le maïs, le riz, la pomme de terre, les légumineuses, le tabac et certains légumes (la tomate, le piment, l’oignon, la carotte). La préparation du sol comprend un labour profond, l’incorporation de compost ou de fumier de ferme (20–50 t/ha), suivis d’un travail du sol léger. Avant la plantation, on épand de l’engrais NPK et, pour assurer une bonne croissance végétative, on fait une application en couverture avec de l’engrais azoté lorsque débute la pommaison. Le type d’engrais et les quantités dépendent du type de sol, des réserves initiales du sol en nutriments et du niveau de rendement. Les taux d’absorption et d’exportation de nutriments sont élevés. Une culture de choux pommés dont le rendement est de 25 t/ha absorbe environ 100 kg de N, 12 kg de P et 75 kg de K. Il est donc recommandé d’au moins doubler cette quantité dans l’apport en engrais. Faire pousser le chou pommé sur des billons pendant la saison humide améliore le drainage. La culture doit être maintenue propre de toute mauvaise herbe, en particulier au cours du mois qui suit le repiquage. Le paillage (d’herbes sèches ou de paille) est favorable à la croissance.
Maladies et ravageurs
Les maladies les plus importantes dans les régions tropicales sont les suivantes : le mildiou (Peronospora parasitica), important surtout à des altitudes supérieures à 1200 m, ainsi que l’alternariose (Alternaria brassicae), contre lesquels on peut lutter à l’aide de fongicides et en choisissant des cultivars tolérants ; la pourriture de la tige (Erwinia carotovora) dans des conditions chaudes et humides ; la nervation noire (Xanthomonas campestris pv. campestris), qui peut être maîtrisée en employant des semences et des plants sains (il existe des cultivars dotés d’un bon niveau de tolérance) et en évitant l’arrosage par aspersion ; le rhizoctone (Rhizoctonia solani), qui provoque la fonte des semis et la nécrose des nervures et des feuilles sous la pomme ; la hernie (Plasmodiophora brassicae), qui constitue une sérieuse menace à des altitudes moyennes (vers 700 m), mais qu’on peut prévenir en procédant à des rotations espacées des cultures, ou à l’éradication des crucifères adventices (plantes-hôtes des agents pathogènes), par chaulage et en installant les cultures sur des sols de pH >7, et enfin en stimulant les champignons antagonistes dans le sol (par ex. Trichoderma et Mortierella spp.). La hernie s’est répandue rapidement au cours des dernières décennies, devenant la maladie la plus préjudiciable dans de nombreuses régions de hautes terres. Quelques cultivars semblent présenter une certaine tolérance mais on ne dispose pas encore de niveaux élevés de résistance durable à la hernie. Les autres maladies sont les suivantes : la maladie des taches noires (Mycosphaerella brassicicola) ; la jaunisse (Fusarium oxysporum f.sp. conglutinans), contre laquelle on lutte par la rotation des cultures et l’emploi de cultivars résistants ; les virus de la mosaïque du navet et du chou-fleur, qu’on peut empêcher en luttant contre leurs vecteurs que sont les pucerons et en éradicant leurs hôtes comme la moutarde sauvage. Une pulvérisation d’alun sur les trognons s’avère efficace pour lutter contre les pourritures d’entreposage provoquées par Erwinia.
Parmi les ravageurs les plus importants, on trouve la teigne des crucifères (Plutella xylostella), contre laquelle la lutte chimique est de plus en plus inefficace car elle devient rapidement résistante à tous les insecticides, à l’exception de ceux à base de nim. Par contre, la lutte biologique à l’aide des phéromones sexuelles et des parasitoïdes (Diadegma semiclausum, Apanteles plutellae, Diadromus collaris et Oomyzus sokolowski) est prometteuse. On trouve ensuite les chenilles tisseuses de pyrales (Crocidolomia binotalis et Hellula undalis), en particulier en Afrique australe. Parmi les ravageurs occasionnels, il faut citer : le ver du cotonnier (Spodoptera littoralis), l’altise (Phyllotreta spp.), la piéride du chou (Pieris spp.) et le puceron cendré du chou (Brevicoryne brassicae). La moutarde brune (Brassica juncea (L.) Czern.), plantée en lignes entre les choux pommés, peut servir de plante-piège pour la teigne des crucifères ainsi que d’autres ravageurs ; la lutte chimique peut alors se limiter aux plantes de moutarde. Les tomates et les oignons constituent d’excellentes cultures répulsives pour la teigne des crucifères.
Récolte
Les pommes, auxquelles on laisse généralement quelques feuilles enveloppantes, sont coupées lorsqu’elles sont bien pleines et fermes, 2–3 mois après le repiquage. La période de récolte s’étale sur 1–2 semaines, les hybrides F1 parvenant à maturité de manière plus uniforme que les variétés-populations. Les rejets latéraux qui se forment sur les trognons décapités donnent des sortes de mini-choux à feuilles lâches qui se récoltent parfois.
Rendements
Les variétés-populations ont un rendement de 10–25 t/ha, et les hybrides F1 de 40–60 t/ha dans des conditions de croissance optimales. Dans les régions tropicales, les meilleurs rendements s’obtiennent généralement au-dessus de 800 m d’altitude. Les rendements en graines atteignent 200–1000 kg/ha en climats tempérés.
Traitement après récolte
Le chou pommé se conserve entre 7–10 jours dans un endroit frais (20°C), bien aéré et à l’obscurité. Le transport doit se faire en caisses ventilées, en filets ou en sacs de jute légers. A 1°C et à un taux d’humidité relative élevé (95–98%), le chou pommé peut se conserver pendant 2–3 mois.
Ressources génétiques
Des collections de ressources génétiques et des collections de travail de chou blanc et d’autres Brassica cultivés sont disponibles dans plusieurs centres de recherche en Europe, en Russie, aux Etats-Unis, en Inde et au Japon. En Europe, une banque de gènes de Brassica a été mise en place en collaboration avec des sociétés privés. Un catalogue électronique central des collections est disponible au Centre for Genetic Resources (CGN) de Wageningen (Pays-Bas). La conservation des ressources génétiques provenant des centres de diversité (la région méditerranéenne) semble adéquate, et les croisements interspécifiques au sein de la famille des Brassicaceae étendent le pool génique accessible aux sélectionneurs.
Sélection
Les programmes actuels d’amélioration génétique visent à produire des hybrides F1 sur la base de croisements simples entre lignées fixées. L’autofécondation s’effectue généralement par pollinisation manuelle du bouton floral ou par traitement au CO2 (2–10%) après une pollinisation par les abeilles, de façon à contourner temporairement l’auto-incompatibilité. On produit aujourd’hui bien plus vite des lignées totalement homozygotes à partir d’haploïdes doublés par culture de microspores, technique mise au point pour Brassica oleracea au début des années 1990.
Les principaux objectifs de sélection concernent : la forme et la taille de la pomme, sa fermeté interne, la configuration et la couleur des feuilles, la longueur du cœur (= la tige interne), le goût, la teneur en vitamine C, la précocité, la tenue sur pied (retard à l’éclatement de la pomme à maturité), la productivité, la tolérance à la chaleur, la résistance aux maladies, aux ravageurs et à la nécrose marginale (désordre physiologique). Des cultivars hybrides F1 dotés d’une bonne résistance à la jaunisse, à la nervation noire et au mildiou ont été mis au point. Cependant, les efforts de sélection pour trouver une résistance durable à la hernie n’ont connu jusqu’ici que des succès limités, en raison de la grande variabilité génétique du pathogène, du nombre limité de sources de résistance et de l’hérédité complexe de la résistance chez les hôtes. Les cultivars de chou pommé reconnus résistants dans une région donnée se montrent souvent sensibles ailleurs en raison de la présence de pathotypes différents de Plasmodiophora brassicae.
La production commerciale de semences d’hybrides F1, traditionnellement obtenue à partir du système de l’auto-incompatibilité, se fait de plus en plus avec une stérilité mâle cytoplasmique (CMS) dans les lignées femelles. Les effets négatifs liés au départ au système de CMS “Ogura” chez Brassica oleracea, tels que la chlorose de la feuille à basses températures, une faible fertilité femelle et une médiocre pollinisation par les insectes en raison de l’absence de glandes nectarifères chez les fleurs, ont été surmontés (par ex. par hybridation avec des protoplastes, suivie d’une sélection stricte parmi les plantes régénérées).
Perspectives
Le chou blanc va prendre de plus en plus d’importance dans les régions tropicales. La tolérance des cultivars à la chaleur permet leur culture à des altitudes moindres, mais les hautes terres continueront à dominer les cultures commerciales, à cause d’un potentiel de rendement plus élevé, d’une meilleure qualité des pommes et de la moindre incidence des maladies et des ravageurs. Les progrès considérables réalisés dans la mise au point de méthodes efficaces de lutte intégrée contre les ravageurs du chou pommé sont susceptibles de diminuer le recours aux pesticides. De plus en plus de cultivars résistants à la jaunisse et à la nervation noire sont disponibles. Cependant, la hernie se répand rapidement dans les régions où l’on pratique le maraîchage intensif et aucun cultivar doté d’une résistance durable ne sera disponible à moyen terme. Les méthodes de lutte au moyen d’antagonistes au pathogène et les méthodes culturales méritent davantage d’attention.
Le développement des marqueurs ADN par les biotechnologies végétales va permettre un criblage indirect plus précis de la résistance aux maladies et aux ravageurs, ainsi que d’autres caractéristiques, et ainsi considérablement augmenter l’efficacité de la sélection chez le chou pommé. Les graines des hybrides japonais sont encore produites principalement par auto-incompatibilité, mais plusieurs semenciers européens et américains se mettent rapidement à adopter le système CMS, en raison de coûts de production inférieurs et de la meilleure qualité des semences (aucune plante autofécondée). Quelques petits semenciers européens qui produisent des semences “biologiques” destinées à l’agriculture biologique refusent d’adopter la CMS dans leur production de graines de Brassica légumiers.
Références principales
- Crisp, P., Crute, I.R., Sutherland, R.A., Angell, S.M., Bloor, K., Burgess, H. & Gordon, P.L., 1989. The exploitation of genetic resources of Brassica oleracea in breeding for resistance to clubroot (Plasmodiophora brassicae). Euphytica 42: 215–226.
- Dickson, M.H. & Wallace, D.H., 1986. Cabbage breeding. In: Bassett, M.J. (Editor). Breeding vegetable crops. Avi Publishing Company, Westport, Connecticut, United States. pp. 395–432.
- Duijs, J.G., Voorrips, R.E., Visser, D.L. & Custers, J.B.M., 1992. Microspore culture is successful in most crop types of Brassica oleracea L. Euphytica 60: 45–55.
- Hervé, Y., 1992. Les choux (Brassica oleracea vegetables). In: Gallais, A. & Bannerot, H. (Editors). Amélioration des espèces végétales cultivées. INRA, Paris, France. pp. 435–447.
- Holland, B., Unwin, I.D. & Buss, D.H., 1991. Vegetables, herbs and spices. The fifth supplement to McCance & Widdowson’s The Composition of Foods. 4th Edition. Royal Society of Chemistry, Cambridge, United Kingdom. 163 pp.
- Nieuwhof, M., 1969. Cole crops: botany, cultivation, and utilization. Leonard Hill, London, United Kingdom. 353 pp.
- Tindall, H.D., 1983. Vegetables in the tropics. Macmillan Press, London, United Kingdom. 533 pp.
- Tsunoda, S., Hinata, K. & Gómez-Campo, C. (Editors), 1980. Brassica crops and wild allies: biology and breeding. Japan Scientific Societies Press, Tokyo, Japan. 354 pp.
- van der Vossen, H.A.M., 1993. Brassica oleracea L. cv. groups White Headed Cabbage, Red Headed Cabbage, Savoy Headed Cabbage. In: Siemonsma, J.S. & Kasem Piluek (Editors). Plant Resources of South-East Asia No 8. Vegetables. Pudoc Scientific Publishers, Wageningen, Netherlands. pp. 117–121.
- Varela, A.M., Seif, A.A. & Loehr, B., 2001. Integrated pest management manual for Brassicas. International Centre of Insect Physiology and Ecology (ICIPE), Nairobi, Kenya. 44 pp.
Autres références
- Bannerot, H., Boulidard, L. & Chupeau, Y., 1997. Unexpected difficulties met with radish cytoplasm in Brassica oleracea. Cruciferae Newsletter 2: 16.
- Charleston, D.S. & Kfir, R., 2000. The possibility of using Indian mustard, Brassica juncea, as a trap crop for the diamond-back moth, Plutella xylostella, in South Africa. Crop Protection 19(7): 455–460.
- Grubben, G.J.H., 1977. Tropical vegetables and their genetic resources. IBPGR, Rome, Italy. 197 pp.
- Imtyiaz, M., Mgadla, N.P., Chepete, B. & Manase, S.K., 2000. Response of six vegetable crops to irrigation schedules. Agricultural Water Management 45(3): 331–342.
- Manzanares-Dauleux, M.J., Divaret, I., Baron, F. & Thomas, G., 2000. Evaluation of French Brassica oleracea landraces for resistance to Plasmodiophora brassicae. Euphytica 113: 211–218.
- Mithen, R.F., 2001. Glucosinolates and their degradation products. Advances in Botanical Research 35: 214–262.
- Pelletier, G., Férault, M., Lancelin, D., Boulidard, L., Doré, C., Bonhomme, S., Grelon, M. & Budar, F., 1995. Engineering of cytoplasmic male sterility in vegetables by protoplast fusion. Acta Horticulturae 392: 11–17.
- Rubatzky, V.E. & Yamaguchi, M., 1997. World vegetables: principles, production and nutritive values. 2nd Edition. Chapman & Hall, New York, United States. 843 pp.
- Talekar, N.S. (Editor), 1992. Diamondback moth and other crucifer pests: Proceedings of the 2nd International Workshop, Tainan, Taiwan, 10-14 December 1990. AVRDC Publication 92-368. AVRDC, Tainan, Taiwan. 603 pp.
- Verkerk, R., 2002. Evaluation of glucosinolate levels throughout the production chain of Brassica vegetables, toward a novel predictive modelling approach. Thesis Wageningen University, Wageningen, Netherlands. 136 pp.
- Voorrips, R.E., 1996. Clubroot in the cole crops: the interaction between Plasmodiophora brassicae and Brassica oleracea. Thesis, Wageningen Agricultural University, Wageningen, Netherlands. 118 pp.
- Voorrips, R.E., Jongerius, M.C. & Kanne, H.J., 2003. Quantitative trait loci for clubroot resistance in Brassica oleracea. In: Nagata, T. & Tabata, S. (Editors). Brassicas and legumes. From genomestructure to breeding. Biotechnology in Agriculture and Forestry 52. Springer Verlag, Berlin, Germany. pp. 87–104.
- Walangululu, J.M. & Mushagalusa, G.N., 2000. The major pests of cabbage (Brassica oleracea var. capitata subs. sabauda) in Bukavu and around. Tropicultura 18(2): 55–57.
- Walters, T.W., Mutschler, M.A. & Earle, E.D., 1991. Protoplast fusion-derived Ogura male sterile cauliflower with cold tolerance. Plant Cell Reports 10(12): 624–628.
Sources de l’illustration
- van der Vossen, H.A.M., 1993. Brassica oleracea L. cv. groups White Headed Cabbage, Red Headed Cabbage, Savoy Headed Cabbage. In: Siemonsma, J.S. & Kasem Piluek (Editors). Plant Resources of South-East Asia No 8. Vegetables. Pudoc Scientific Publishers, Wageningen, Netherlands. pp. 117–121.
Auteur(s)
- H.A.M. van der Vossen, Steenuil 18, 1606 CA Venhuizen, Netherlands
- A.A. Seif, ICIPE, P.O. Box 30772, Nyago Stadium, Nairobi, Kenya
Basé sur PROSEA 8: ‘Vegetables’.
Citation correcte de cet article
van der Vossen, H.A.M. & Seif, A.A., 2004. Brassica oleracea L. (chou pommé) In: Grubben, G.J.H. & Denton, O.A. (Editeurs). PROTA 2: Vegetables/Légumes. [CD-Rom]. PROTA, Wageningen, Pays Bas.
Consulté le 17 décembre 2024.