Allium fistulosum (PROTA)
Introduction |
| Importance générale | |
| Répartition en Afrique | |
| Répartition mondiale | |
| Glucides / amidon | |
| Médicinal | |
| Ornemental | |
| Fourrage | |
| Sécurité alimentaire | |
- Protologue: Sp. pl. 1 : 301 (1753).
- Famille: Alliaceae
- Nombre de chromosomes: 2n = 16
Noms vernaculaires
- Ciboule (Fr).
- Welsh onion, Japanese bunching onion (En).
- Cebolinha, cozida (Po).
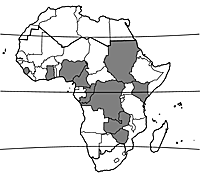
Origine et répartition géographique
Allium fistulosum n’est connu qu’à l’état cultivé et est probablement originaire du nord-ouest de la Chine. Des études sur son ADN indiquent qu’il dérive de l’espèce sauvage Allium altaicum Pall., que l’on rencontre en Sibérie et en Mongolie, où elle est parfois récoltée comme légume sauvage pour l’usage local ou pour l’exportation en Chine. La culture d’Allium fistulosum en Chineremonte au moins à 200 ans avant J.-C. Elle a été introduite au Japon avant l’an 500 de notre ère, et s’est ensuite diffusée en Asie du Sud-Est et en Europe. Le nom anglais de “welsh onion” n’a pas de lien direct avec le pays de Galles au Royaume-Uni, mais s’apparente au vieil allemand “welsche” qui signifiait “étranger”. En Chine, Allium fistulosum est l’espèce d’Allium la plus importante, jouant à la fois le rôle de l’oignon et du poireau dans la cuisine européenne ; au Japon, elle vient aujourd’hui au second rang après l’oignon (Allium cepa L.). La plante est cultivée dans le monde entier, mais sa principale zone de culture reste l’Asie orientale, de la Sibérie à l’Indonésie ; ailleurs, on la trouve surtout dans les jardins familiaux. En Afrique, elle n’est importante que localement, et elle est signalée en Sierra Leone, au Ghana, au Cameroun, au Congo, en R.D. du Congo, au Soudan, au Kenya, en Zambie et au Zimbabwe. Un “oignon” cultivé pour son feuillage au Nigeria appartient probablement aussi à Allium fistulosum.
Usages
On cultive deux types d’Allium fistulosum, parfois distingués comme groupes de cultivars : le groupe Ciboule orientale ou Japanese Bunching et le groupe Ciboule européenne ou Welsh Onion. La ciboule orientale est surtout cultivée en Asie orientale pour ses pseudo-tiges étiolées et épaisses, consommées comme légume cuit pour le sukiyaki ou pour des plats à base de poulet. La ciboule européenne est cultivée pour ses feuilles vertes, utilisées dans des salades, ou comme herbe condimentaire pour donner du goût aux soupes ou à d’autres plats. C’est cette dernière qui est la plus commune en Afrique. Dans la zone de Brazzaville-Kinshasa (Congo et R.D. du Congo), on récolte les plantes entières et on les consomme en légume bouilli. En Asie du Sud-Est (Java), on consomme aussi les plantes entières, cuites à la vapeur ou brièvement passées à la poële. Au Japon, on utilise des plantules de 7–10 cm de haut pour des plats spéciaux. Ce n’est que récemment qu’Allium fistulosum a été utilisé par l’industrie, sous forme déshydratée. Le produit est utilisé surtout comme additif à des plats préparés, comme les nouilles instantanées. Les jeunes inflorescences sont parfois consommées frites en amuse-gueule.
Les plantes sont réputées réduire ou prévenir l’invasion des jardins par les termites. Leur jus dilué est utilisé en Chine pour lutter contre les pucerons. On attribue à Allium fistulosum de nombreuses propriétés médicinales, surtout en médecine chinoise. On l’utilise pour améliorer le fonctionnement des organes internes et le métabolisme, pour prévenir les maladies cardiovasculaires et pour prolonger la vie. Elle améliorerait aussi la vue, et contribuerait à la guérison des rhumes, des maux de tête, des blessures et des ulcères purulents.
Production et commerce international
Il n’existe pas de statistiques mondiales pour Allium fistulosum, car les données sur sa production sont souvent confondues avec celles d’autres Allium. La Chine, le Japon, la Corée, Taïwan et l’Indonésie sont les principaux producteurs. In 1984, la production au Japon atteignait 563 000 t sur 24 000 ha, en Corée 432 000 t sur 19 000 ha.
Propriétés
La composition nutritionnelle des feuilles vertes crues est, par 100 g de partie comestible : eau 90,5 g, énergie 142 kJ (34 kcal), protéines 1,9 g, lipides 0,4 g, glucides 6,5 g, Ca 18 mg, Mg 23 mg, P 49 mg, Fe 1,2 mg, Zn 0,52 mg, vitamine A 1160 UI, thiamine 0,05 mg, riboflavine 0,09 mg, niacine 0,40 mg, folates 16 μg, acide ascorbique 27 mg (USDA, 2002). La valeur nutritionnelle des feuilles vertes est plus élevée que celle des pseudo-tiges étiolées.
L’odeur d’Allium fistulosum n’est pas très forte. Du point de vue chimique, elle est intermédiaire entre celles de l’oignon et du poireau. Elle dérive du propyl cystéine sulfoxyde (caractéristique du poireau) et du propényl cystéine sulfoxyde (caractéristique de l’oignon), qui sont volatiles. Ces alkyl-sulfoxydes sont des produits de dégradation d’acides aminés non-protéiques du groupe des S-alk(én)yl-cystéines. Quand les cellules sont endommagées, les acides aminés se dégradent, sous l’action de l’enzyme aliinase, en acides sulféniques très réactifs, ammoniaque et pyruvate. Les acides sulféniques réagissent ensuite avec d’autres substances pour former divers disulfures.
Une forte proportion des glucides de réserve est constituée de sucres et d’oligosaccharides. Outre le glucose, le fructose et le saccharose, on trouve aussi du maltose, du rhamnose, du galactose, de l’arabinose, du mannose et du xylose. La teneur en sucres et en protéines s’accroît chez les plantes poussant à température plus basse, ce qui améliore leur qualité alimentaire.
Des expériences ont montré que des extraits de ciboule peuvent moduler le tonus vasculaire in vitro dans les aortes thoraciques de rats. Cela justifie leur usage en médicine traditionnelle pour prévenir les maladies cardiovasculaires. Des substances antifongiques ont été extraites des graines.
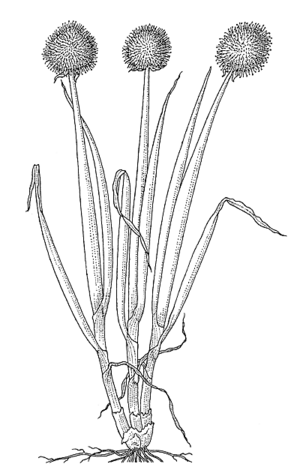
Description
- Plante herbacée vivace, glabre, poussant en touffes, habituellement cultivée comme annuelle ou bisannuelle, atteignant 50(–100) cm de haut, à bulbe indistincte ovoïde à oblongoïde jusqu’à 10 cm de long, bulbes latéraux plus ou moins nombreux ou pratiquement absents ; tunique blanche à brun rougeâtre pâle.
- Feuilles 4–12, alternes distiques, glauques, à gaine tubulaire ; limbe cylindrique, creux, de 10–50(–100) cm × 0,5–2,5 cm, aigu à l’apex.
- Inflorescence : ombelle sphérique de 3–7 cm de diamètre, sur une hampe longue, érigée, cylindrique et creuse, atteignant 50(–100) cm de long et 2,5 cm de diamètre ; ombelle composée soit de fleurs soit uniquement de bulbilles ; spathe 1, hyaline, persistante, jusqu’à 1 cm de long, se fendant en (1–)2–3 parties.
- Fleurs bisexuées, étroitement campanulées ou urcéolées ; pédicelle fin, jusqu’à 3 cm de long ; tépales 6, en 2 verticilles, libres, ovales-oblongs à oblongs-lancéolés, de 6–10 mm de long, blancs avec une nervure médiane verdâtre ; étamines 6, dépassant les tépales, connées à la base et adnées aux tépales ; ovaire supère, 3-loculaire, style fin, dépassant les tépales.
- Fruit : capsule globuleuse d’environ 5 mm de diamètre, à déhiscence loculicide, contenant peu de graines.
- Graines de 3–4 mm × 2–2,5 mm, noires.
Autres données botaniques
En Europe, une classification en 2 groupes de cultivars a été proposée : le groupe Ciboule orientale (en anglais Japanese Bunching), cultivars à tige unique cultivés pour leur fausse-tige épaisse ; et le groupe Ciboule européenne (en anglais Welsh Onion), cultivars à nombreuses tiges cultivés pour leurs feuilles. Une classification en 3 groupes est commune au Japon : le groupe Kaga est cultivé dans les zones fraîches du Japon pour ses fausses-tiges ; le groupe Kujyo est surtout cultivé dans les zones chaudes du Japon, et surtout pour ses feuilles ; et le groupe Senju, intermédiaire pour ses usages et ses exigences écologiques.
Superficiellement, Allium fistulosum ressemble beaucoup à Allium cepa, mais il ne forme pas de bulbe, bien qu’un léger renflement à la base de la fausse-tige puisse se manifester. Les feuilles sont de section plus circulaire, sans aplatissement adaxial. Les différences sont encore plus évidentes pour les fleurs. Chez Allium fistulosum, la floraison procède du haut vers le bas de l’ombelle. Les fleurs n’ont pas de bractéoles, sont plus grandes et campanulées à urcéolées, alors que celles d’Allium cepa ont des bractéoles, et sont plus petites et étoilées.
Allium fistulosum s’hybride facilement avec Allium altaicum ; les hybrides montrent une très bonne fertilité du pollen et produisent de nombreuses graines. L’hybridation est possible aussi avec Allium cepa. Les hybrides sont des plantes vivaces formant de petits bulbes. Plusieurs hybrides anciens sont connus entre Allium fistulosum comme parent femelle et des échalotes tropicales (Allium cepa groupe Aggregatum). On les désigne sous les noms d’Allium ×proliferum, Allium ×wakegi ou Allium fistulosum var. caespitosum. On peut citer l’échalote indonésienne ‘Sumenep’, bien adaptée aux conditions tropicales et qui ne fleurit jamais, et l’oignon vivipare, chez lequel l’inflorescence est composée de bulbilles. Au stade végétatif, ces plantes ressemblent à Allium fistulosum. Des hybrides commerciaux récents entre Allium fistulosum comme parent femelle et Allium cepa, sont cultivés principalement aux Etats-Unis et en Europe pour leurs feuilles vertes, tels que ‘Beltsville Bunching’ (tétraploïde reproduit par graines), ‘Louisiana Evergreen’ (diploïde stérile) et ‘Delta Giant’ (triploïde stérile provenant du recroisement de l’hybride avec Allium cepa). Un autre type d’hybrides cultivé au Japon est le groupe Yakura Negi, dont les plantes tallent abondamment au printemps et en été et restent dormantes en hiver. Leur inflorescence ne produit pas de fleurs mais seulement des bulbilles ; on les multiplie par division de touffes ou grâce aux bulbilles.
Croissance et développement
Allium fistulosum est une plante vivace, surtout cultivée commercialement comme annuelle, mais aussi comme pérenne dans les jardins familiaux. Il n’y a pas, comme chez Allium cepa, de dormance en jours longs, si bien que la plante continue à croître et ne forme pas de bulbe proprement dit. Cependant, certains cultivars provenant de zones tempérées froides montrent une dormance de jours courts. Ils s’arrêtent de croître, leurs feuilles sèchent et meurent en conditions de jours courts, même si la température aurait permis une croissance normale. Les bourgeons latéraux à l’aisselle des feuilles s’allongent et se développent en talles pour former une touffe. Ce caractère est plus prononcé chez les cultivars utilisés en feuilles vertes que chez ceux cultivés pour obtenir de longues fausses-tiges étiolées.
L’induction florale est sous l’influence de la température et de la photopériode. Les températures basses et les jours courts induisent la floraison, mais les conditions nécessaires varient beaucoup avec l’origine des cultivars. La floraison est en général induite par des températures inférieures à 13°C, quand les jeunes plantes ont formé un certain nombre de feuilles ou une fausse-tige suffisamment épaisse. Sous les tropiques, où les conditions de milieu favorisent plutôt la croissance végétative que la reproduction, seuls quelques cultivars spécialement adaptés sont capables de fleurir.
Les racines sont fortement colonisées par des champignons mycorhiziens arbusculaires, ce qui favorise l’absorption des phosphates et stimule la croissance.
Ecologie
Allium fistulosum peut s’adapter à une très large gamme de climats. Très tolérant au froid, il peut survivre à l’hiver même en Sibérie. Il tolère aussi des conditions humides et chaudes comme celles qui règnent à Brazzaville et Kinshasa en Afrique centrale. A Java (Indonésie), il se développe bien à partir de 200 m d’altitude, mais il est plus commun au-dessus de 500 m. La plupart des cultivars locaux sont bien adaptés aux variations de pluviosité, et sont plus tolérants à de très fortes pluies que les autres espèces d’Allium. Des plantes bien enracinées tolèrent des périodes de stress hydrique, et la sécheresse ne les fera mourir que rarement.
Un sol bien drainé, limoneux, riche en matière organique, sera l’idéal. Allium fistulosum est très sensible à l’asphyxie racinaire, qui tue rapidement les racines actives. La meilleure végétation est obtenue en sol de pH neutre, mais même à pH 8–10, une bonne croissance est possible. En sol acide, la végétation est en général chétive.
Multiplication et plantation
Sous les tropiques, Allium fistulosum est multiplié principalement grâce à des rejets à la base de la plante, et peut être ainsi planté toute l’année. Bien que la production de graines soit possible à des altitudes supérieures à 1000 m, et que l’on dispose aussi de semences importées de cultivars taïwanais et japonais, on reproduit rarement la ciboule par graines car c’est plus difficile en conditions tropicales, et cela demande plus de temps. Cependant, dans la zone de Brazzaville-Kinshasa, on utilise aussi bien les graines que les rejets des cultivars locaux. Dans les zones tempérées où la production de graines réussit mieux, on multiplie surtout par graines, que l’on sème soit directement au champ soit d’abord en pépinière. Le poids de 1000 graines est de 2,2–2,5 g. Il faut 8–16 kg/ha en semis direct et 2–4 kg/ha s’il y a repiquage. En pépinière, les graines sont semées soit à la volée, soit en lignes, ou en bandes de 5–6 cm de large. La superficie de la pépinière sera de 10–12% de celle du champ. Les plants sont bons à repiquer quand ils sont hauts de 25–30 cm et de l’épaisseur d’un crayon.
Gestion
Pour produire du feuillage, la préparation du sol n’a pas besoin d’être profonde. Les rejets ou plants sont repiqués sur des planches surélevées ou sur des billons, alternant avec des rigoles pour l’irrigation ou le drainage. Les distances de plantation sont d’environ 20 cm × 25 cm (200 000 plantes par ha). On raccourcit en général d’un tiers la partie supérieure des plants pour réduire la transpiration. Les trous de plantation sont remplis avec 50–100 g de fumier (10–20 t/ha) et les plants insérés obliquement pour stimuler le tallage. De l’urée ou du sulfate d’ammoniaque à raison de 3 g par plante (environ 600 kg/ha) est appliqué 3 semaines après plantation, et de nouveau 6 semaines après plantation si le sol est peu fertile. On désherbe et on butte en général 6–7 semaines après la plantation. Allium fistulosum demande beaucoup d’eau. A basse altitude, il est habituellement cultivé pendant la saison des pluies. Il faut arroser tous les jours pendant la saison sèche. En altitude, on pratique souvent la culture associée, avec choux, carottes et pommes de terre.
Pour produire de fausses-tiges étiolées, on travaille le sol plus profondément. On fait des sillons de 10–20 cm de profondeur, en rejetant le sol sur un côté pour former un billon qui soutiendra la jeune plante et facilitera le buttage ultérieurement. Ce buttage est essentiel pour blanchir et rendre plus tendre le cylindre formé par les gaines foliaires. Mais comme le buttage nuit à l’aération des racines, retardant ainsi la croissance, on le pratiquera progressivement et pas trop tôt.
Maladies et ravageurs
Les cultures d’Allium fistulosum sont en général en bon état sanitaire, mais il peut être atteint par un certain nombre de maladies, dont la plupart sont les mêmes que celles des autres Allium cultivés. L’alternariose (Alternaria porri), qui provoque des taches zonées concentriquement sur les feuilles, et le mildiou (Peronospora destructor) peuvent poser de sérieux problèmes. La pourriture blanche (Sclerotium cepivorum) peut provoquer de graves pertes en cas de cultures successives ou répétées, car ce pathogène est très persistant dans le sol. Une nutrition insuffisante ou déséquilibrée, ainsi que de fortes pluies, peuvent stimuler le développement des maladies. La pratique de la multiplication végétative favorise les attaques de virus, mais beaucoup de variétés locales semblent relativement tolérantes. Les plantes malades seront éliminées grâce à une inspection visuelle rigoureuse du matériel de plantation. Allium fistulosum est résistant au virus de la bigarrure de l’oignon (OYDV), mais sensible au virus de la striure jaune de la ciboule (WoYSV), qui sévit par exemple au Japon et en Indonésie, et qui provoque des symptômes analogues de type mosaïque : marbrure chlorotique, striure, nanisme et distorsion des feuilles épaissies. Les cultivars du groupe Kujyo sont relativement tolérants.
Allium fistulosum est résistant à plusieurs maladies qui attaquent les autres Allium, dont la maladie des racines roses due à Pyrenochaeta terrestris, les pourritures causées par Botrytis spp. et les taches foliaires provoquées par Botrytis squamosa. On a trouvé une résistance partielle à l’anthracnose (Colletotrichum gloeosporioides).
Les noctuelles Spodoptera exigua et Heliothis armigera sont les insectes les plus nuisibles. La lutte est difficile car les chenilles se cachent dans les feuilles creuses, et la cire qui couvre les feuilles les rend difficilement mouillables. Le thrips de l’oignon (Thrips tabaci) peut provoquer d’importants dommages, qui peuvent être accentués par les pulvérisations contre Spodoptera, car celles-ci éliminent les ennemis naturels des thrips. Par contre, l’arrosage par aspersion peut réduire les dégâts du thrips.
Récolte
Sous les tropiques, Allium fistulosum peut être récolté tout au long de l’année ; dans la zone Brazzaville-Kinshasa, on récolte principalement en saison des pluies. On arrache environ 2,5 mois après le repiquage. On laisse en place ce qu’il faut pour la plantation suivante jusqu’à ce qu’on en ait besoin. La récolte demande beaucoup de travail, surtout s’il s’agit de fausses-tiges, que l’on doit arracher à la bêche, nettoyer et lier en bottes. Au Japon, on a mis au point l’équipement nécessaire pour une récolte mécanique.
Rendement
On ne dispose pas de données à ce sujet pour l’Afrique. Les rendements moyens au Japon et en Corée sont d’environ 25 t/ha, à Taïwan de 10–15 t/ha. En Indonésie, ils sont beaucoup plus faibles, en moyenne 7 t/ha, pouvant atteindre 15 t/ha ; il faut cependant remarquer que cette récolte est obtenue en seulement 2,5–3 mois, au lieu de 9 mois dans l’est de l’Asie.
Traitement après récolte
Après la récolte, les feuilles et les fausses-tiges sont nettoyées et séchées, on enlève les feuilles en mauvais état, et les plantes sont liées en bottes et empaquetées dans des cageots ou des paniers pour le transport au marché.
Ressources génétiques
Des collections de ressources génétiques sont maintenues au Japon, aux Etats-Unis, au Royaume-Uni, en Allemagne et dans l’ex-URSS. L’IPGRI place Allium fistulosum au second rang pour son importance dans le genre Allium, à cause de ses résistances aux maladies, de sa vaste adaptation écologique et de sa proche parenté avec Allium cepa. Les sélectionneurs entretiennent souvent leur propres collections et font des échanges, maintenant ainsi un niveau de variabilité satisfaisant.
Sélection
Dans la plupart des pays, les paysans produisent eux-mêmes graines ou matériel de plantation. Au Japon, une filière semencière s’est développée, et plusieurs nouveaux cultivars sont diffusés chaque année. Il y a aussi d’importants programmes de sélection en Chine et à Taïwan. Les buts des sélectionneurs sont d’améliorer l’homogénéité des cultivars ainsi que l’adaptation à diverses conditions écologiques. Pour les cultivars destinés à produire des fausses-tiges, l’objectif est d’obtenir des lignées présentant le moins possible de tallage. Des lignées mâle-stériles sont disponibles, et des hybrides F1 ont été proposés.
Perspectives
Les grandes facultés d’adaptation de l’espèce, et l’exemple du Japon et de Taïwan, où l’intensification de la culture, combinée avec un travail de sélection améliorante et le développement d’un bon réseau commercial, a conduit à une expansion considérable de la production, indiquent qu’il y a de bonnes perspectives pour la mise au point de meilleurs cultivars et pour des progrès dans la commercialisation et une intensification de la production sous les tropiques, y compris pour l’Afrique.
Références principales
- de Wilde-Duyfjes, B.E.E., 1976. A revision of the genus Allium L. (Liliaceae) in Africa. Mededelingen Landbouwhogeschool Wageningen 76–11. Wageningen, Netherlands. 239 pp.
- Helm, J., 1956. Die zu Würz- und Speisezwecken kultivierten Arten der Gattung Allium L. Kulturpflanze 4: 130–180.
- Inden, H. & Asahira, T., 1990. Japanese bunching onion (Allium fistulosum L.). In: Brewster, J.L. & Rabinowitch, H.D. (Editors). Onions and allied crops. Volume 3. CRC Press, Boca Raton, Florida, United States. pp. 159–178.
- Jones, H.A. & Mann, L.K., 1962. Onions and their allies. Leonard Hill, London, United Kingdom. 286 pp.
- Krug, H., Berg, E., Crüger, G. & Fölster, E., 1991. Gemüseproduktion: ein Lehr- und Nachschlagewerk für Studium und Praxis. 2nd edition. Verlag Paul Parey, Berlin, Germany. 541 pp.
- Moore Jr, H.E., 1955. Cultivated Alliums. Baileya 3: 156–167.
- Oyen, L.P.A. & Soenoeadji, 1993. Allium fistulosum L. In: Siemonsma, J.S. & Kasem Piluek (Editors). Plant Resources of South-East Asia No 8. Vegetables. Pudoc Scientific Publishers, Wageningen, Netherlands. pp. 73–77.
- Shinohara, S., 1980. Guidebook for development of vegetable horticulture with capable seed production in the monsoon subtropics. Shinohara's Authorized Agricultural Consulting Engineer Office, Tokyo, Japan. 218 pp.
- Takamatsu, E., 1989. Leaf onion, Allium fistulosum. In: Shinohara, S. (Editor): Vegetable seed production technology of Japan. Volume 2. Shinohara's Authorized Agricultural Consulting Engineer Office, Tokyo, Japan. pp. 260–287.
Autres références
- Arifin, N.S., Ozaki, Y. & Okubo, H., 2000. Genetic diversity in Indonesian shallot (Allium cepa var. ascalonicum) and Allium × wakegi revealed by RADP markers and origin of A. × wakegi identified by RFLP analyses of amplified chloroplast genes. Euphytica 111: 23–31.
- Chen, J.H., Tsai, S.J. & Chen, H.I., 1999. Welsh onion (Allium fistulosum L.) extracts alter vascular responses in rat aortae. Journal of Cardiovascular Pharmacology 33(4): 515–520.
- Currah, L. & Proctor, F., 1990. Onions in tropical regions. NRI, Greenwich, United Kingdom. 232 pp.
- Diekman, M. (Editor), 1997. FAO/IPGRI Technical guidelines for the safe movement of germplasm. No 18. Allium spp. Food and Agriculture Organization (FAO) and International Plant Genetic Resources Institute (IPGRI), Rome, Italy. 60 pp.
- Friesen, N., Pollner, S., Bachmann, K. & Blattner, F.R., 1999. RAPDs and noncoding chloroplast DNA reveal a single origin of the cultivated Allium fistulosum from A. altaicum (Alliaceae). American Journal of Botany 86: 554–562.
- Galván, G.A., Wietsma, W.A., Putrasemedja, S., Permadi, A.H. & Kik, C., 1997. Screening for resistance to anthracnose (Colletotrichum gloeosporioides Penz.) in Allium cepa and its wild relatives. Euphytica 95: 173–178.
- Hetterscheid, W.L.A., van Ettekoven, C., van den Berg, R.G. & Brandenburg, W.A., 1999. Cultonomy in statutory registration exemplified by Allium L. crops. Plant Varieties and Seeds 12: 149–160.
- Messiaen, C.-M., 1989. Le potager tropical. 2nd Edition. Presses Universitaires de France, Paris, France. 580 pp.
- Messiaen, C.-M., Cohat, J., Leroux, J.P., Pichon, M. & Beyries, A., 1993. Les Allium alimentaires reproduits par voie végétative. INRA éditions. 230 pp.
- Pino, J.A., Rosado, A. & Fuentes, V., 2000. Volatile flavor compounds from Allium fistulosum L. Journal of Essential Oil Research 12: 553–555.
- Tawaraya, K., Tokairin, K. & Wagatsuma, T., 2001. Dependence of Allium fistulosum cultivars on the arbuscular mycorrhyzal fungus, Glomus fasciculatum. Applied Soil Ecology 17(2): 119–124.
- USDA, 2002. USDA nutrient database for standard reference, release 15. [Internet] U.S. Department of Agriculture, Beltsville Human Nutrition Research Center, Beltsville Md, United States. http://www.nal.usda.gov/fnic/foodcomp. June 2003.
- Yamasaki, A., Miura, H. & Tanaka, K., 2000. Effect of photoperiods before, during and after vernalization on flower initiation and development and its varietal difference in Japanese bunching onion (Allium fistulosum L.). Journal of Horticultural Science and Biotechnology 75: 645–650.
- Yamasaki, A., Tanaka, K., Yoshida, M. & Miura, H., 2000. Effects of day and night temperatures on flower-bud formation and bolting of Japanese bunching onion (Allium fistulosum L.). Journal of the Japanese Society of Horticultural Science 69: 40–46.
Sources de l'illustration
- Oyen, L.P.A. & Soenoeadji, 1993. Allium fistulosum L. In: Siemonsma, J.S. & Kasem Piluek (Editors). Plant Resources of South-East Asia No 8. Vegetables. Pudoc Scientific Publishers, Wageningen, Netherlands. pp. 73–77.
Auteur(s)
- L.P.A. Oyen, PROTA Network Office Europe, Wageningen University, P.O. Box 341, 6700 AH Wageningen, Netherlands
- C.-M. Messiaen, Bat. B 3, Résidence La Guirlande, 75, rue de Fontcarrade, 34070 Montpellier, France
Consulté le 18 décembre 2024.