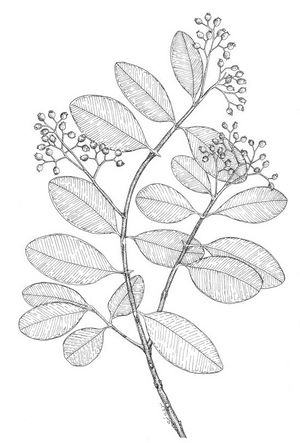
Pimenta racemosa (TRAMIL)
| |
- Nom accepté : Pimenta racemosa
- Voir sur la TRAMILothèque (davantage d’illustrations)
Sommaire
Noms vernaculaires significatifs TRAMIL
- La Dominique : bay-run, bwaden
- Rép. Dominicaine : bay run, berrón
- autres noms créoles : bois d’inde, bwa-béronm, fèy ésans jiwof, malaguette
Distribution géographique
Originaire du Nord de l’Amérique du Sud et des Antilles, cultivée sous les tropiques.
Description botanique
Arbre pouvant atteindre 15 m de haut, écorce grisâtre à marron clair, se détache en fines couches. Feuilles elliptiques oblongues ou obovées, obtuses à la base et émarginées à la pointe, glabres à nervation finement réticulée, points pellucides glandulaires. Panicules en corymbe terminales ou sous-terminales; avec fleurs blanches ou roses, glanduleuses, ayant plusieurs étamines; calice à 5 lobes, larges et triangulaires. Fruit ovoïde allant jusqu’à 1 cm, noir à maturité.
Voucher : Jiménez,60,JBSD
Emplois traditionnels significatifs TRAMIL
- mal de dents : feuille écrasée[1], application locale1
- rhumatismes : feuille écrasée, massage local2
- ↑ fréquemment associée à Allium sativum et Syzygium aromaticum
Recommandations
Selon l’information disponible :
L’emploi contre le mal de dents et les rhumatismes est classé REC sur la base de l’usage significatif traditionnel documenté par les enquêtes TRAMIL et l’information scientifique publiée.
Toute application locale doit se conformer à de strictes mesures d’hygiène pour éviter la contamination et une infection surajoutée.
L’emploi de ce remède contre le mal de dents doit être considéré comme un complément au traitement odontologique.
La feuille peut produire des réactions d’hypersensibilité.
Ne pas avaler la feuille ni employer avec des femmes enceintes ou allaitantes, ni avec des enfants de moins de 5 ans.
Chimie
La feuille contient de l’huile essentielle : eugénol, iso-eugénol-trans-méthyl éther, 1-8 cinéol, thymol, limonène, γ-terpinène, ρ-cymén-8-ol, myrcène, transsabinène, α-terpinène, chavicol3.
L’huile essentielle de la feuille contient 3-diméthoxyallilbenzène et constitue 1-3% du poids du végétal frais4. 4-méthoxy-isoeugénol (75,2%), 4-méthoxy-eugénol (4,5%)5, terpinén-4-ol, 1,8-cinéol, eugénol, chavicol, α-terpinéol6.
Il existe 3 variétés très proches du point de vue chimiotaxonomique, la plus commune étant la variété grisea, les deux autres diffèrent par l’odeur de la feuille et, de ce fait, par la nature des huiles essentielles qu’elles contiennent. L’huile essentielle de la feuille contient 3-diméthoxyallylbenzène et constitue 1-3% du poids du végétal frais.
Pour la variété grisea, les constituants chimiques peuvent être classés en 3 groupes :
- hydrocarbures monoterpéniques : myrcène (majoritaire), allo-cymène, limonène, α-phélandrène, dipentène (minoritaires) ;
- monoterpènes aldéhydiques : citral, citronellal et géranial ;
- éthers phénoliques : eugénol (majoritaire), méthyleugénol, chavicol, 3-4 diméthoxyallylbenzène, méthyl chavicol (minoritaires).
Cette composition reste relativement constante en fonction du lieu ou de la période de récolte. La variété sentant le citral est très riche de ce composant et contient peu d’eugénol. La variété sentant l’anis ne contient pas non plus de quantités appréciables d’eugénol et est caractérisée par son contenu en dérivés du chavicol et du méthyl-eugénol4,7.
La distillation à la vapeur de la branche donne un maximum de 3,9% d’huile essentielle, dont le composant majoritaire est l’eugénol (environ 56%), le chavicol (22%) et le myrcène (21%); tandis que les variétés anisées contiennent approximativement 43% de méthyleugénol et 32% de méthyl-chavicol et les variétés avec prédominance de l’odeur citronnée se caractérisant par un contenu où domine le citral, lequel peut dépasser 80% du contenu total de l’huile essentielle7.
Activités biologiques
On attribue à l’eugénol des propriétés antiseptiques, anesthésique locale, analgésique dentaire8-9, spasmolytique, parasympathicholitique et vasodilatatrice périphérique10. On a constaté que le 3-4 diméthoxyallilbenzène exerçait une activité calmante et narcotique sur des modèles expérimentaux sur souris et poisson et qu’il protégeait contre les convulsions induites par strychnine11-12.
On ne dispose pas d’information, dans la littérature scientifique, pour la validation des effets attribués à la feuille écrasée en application locale ou en massage local contre les douleurs dentaires et les rhumatismes.
Toxicité
Travail TRAMIL13
L’extrait aqueux (décoction 10 minutes, neutralisée chimiquement à pH 7) de feuille séchée et moulue, par voie intrapéritonéale à la souris, avec une observation de 10 jours, a montré une DL50 de 2,08 ± 0,27 g/kg. Par voie orale, les doses de 6,25; 12,5 et 18,75 g de matière végétale sèche/kg à la souris, quotidiennement pendant 30 jours, n’ont pas provoqué de toxicité.
Travail TRAMIL3
L’huile essentielle de plante entière, par voie orale, dose non létale à la souris, a montré qu’elle provoquait des lésions dans l’appareil digestif. A des doses plus fortes, l’observation anatomopathologique a montré la présence d’ulcères ouverts, une nécrose de l’estomac et une hémorragie intestinale. La DL50 de l’huile essentielle de plante entière par voie orale à la souris a été de 443 mg/kg.
L’extrait aqueux de feuille in vitro n’a pas eu d’effet mutagène12.
La DL50 de l’eugénol, par voie orale au rat, a été de 2,68 g/kg et à la souris, elle a été de 3 g/kg14.
L’eugénol contenu dans l’huile essentielle est irritant et peut induire des réactions d’hypersensibilité15.
On ne dispose pas d’information permettant d’établir l’innocuité de son emploi médicinal avec des enfants, ni avec des femmes enceintes ou allaitantes.
Préparation et dosage
La feuille de Pimenta racemosa est une source industrielle d’huile essentielle.
Contre le mal de dents :
Laver soigneusement la feuille, l’écraser avec un bouton floral avant son ouverture et séché de Syzygium aromaticum (clou de girofle) et une gousse d’Allium sativum (ail); appliquer 5-10 grammes de matière végétale ainsi préparée sur la dent affectée, 2-3 fois par jour16.
Contre les rhumatismes :
Laver soigneusement la feuille, l’écraser, prendre 30 grammes de matière végétale et frictionner pendant 2-5 minutes la peau de la zone affectée, 2 fois par jour16.
Toute préparation médicinale doit être conservée au froid et utilisée dans les 24 heures.
Références
- GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984 Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
- CHARLES C, 1988 TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
- BOURGEOIS P, 1986 Rapport concernant Pimenta racemosa (Myrtacées). Rapport TRAMIL. Laboratoire de phytochimie, Faculté des Sciences, UAG, Guadeloupe.
- FURIA T, BELLANCA N, 1971 Fenaroli’s handbook of flavour ingredients. Cleveland, USA: The Chemical Rubber Co.
- GARCIA D, ALVAREZ A, TORNOS P, FERNANDEZ A, SÁENZ T, 2002 Gas chromatographic-mass spectrometry study of the essential oils of Pimenta racemosa var. terebinthina and P. racemosa var grisea. Z Naturforsch C 57(5-6):449-451.
- LEYVA M, TARACONTE J, MARQUETTI MdC, 2007 Composición química y efecto letal del aceite esencial de Pimenta racemosa (Myrtales: Myrtaceae) sobre Blattella germanica (Dictyoptera: Blattellidae). Rev Cubana Med Trop 59(2):154-158.
- LEUNG AY, FOSTER S, 1980 Encyclopedia of common natural ingredients used in food, drugs and cosmetics. New York, USA: Wiley Interscience.
- NEGWER M, 1987 Organic chemical drugs and their synonyms (an international survey), 6th ed. Berlin, Germany: Akademie Verlag.
- DUKE JA, 1992 Handbook of biologically active phytochemicals and their bioactivities. Boca Raton, USA: CRC Press.
- DE SOUSA M, MATOS ME, MATOS FJ, MACHADO MI, CRAVEIRO AA, 1991 Constituintes químicos ativos de plantas medicinais Brasileiras. Fortaleza, Brasil: Ceará Edições UFC Laboratorio de produtos naturais.
- MAC GREGOR JT, LAYTON LL, BUTTERY RG, 1974 California bay oil. II. Biological effects of constituents. J Agric Food Chem 22(5):777-780.
- UNGSURUNGSIE M, SUTHIENKUL O, PAOVALO C, 1982 Mutagenicity screening of popular Thai spices. Food Chem Toxicol 20(5):527-530.
- HERRERA J, 1988 Determinación de actividades biológicas de vegetales utilizados en medicina tradicional. Informe TRAMIL. Dep. de Farmacología, Facultad de Salud, Universidad del Valle, Cali, Colombia.
- BUDAVARI S (Ed.), 2001 The Merck Index: an encyclopedia of chemicals, drugs, and biologicals. 30th ed. Whitehouse Station, USA: Merck & Co., Inc. p690.
- REYNOLDS J (Ed.), 1996 Martindale: The extra pharmacopoeia. 31st ed. London, England: The Royal Pharmaceutical Society. p1705.
- CARBALLO A, 1995 Cálculo de concentración y dosis de las drogas vegetales TRAMIL: Mensuraciones farmacognósticas y aproximaciones técnico-clínicas. Laboratorio provincial de producción de medicamentos, Sancti Spiritus, Cuba.