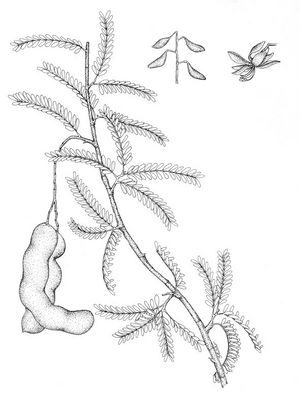
Tamarindus indica (TRAMIL)
| |
= Tamarindus officinalis Hook. = Tamarindus umbrosa Salisb.
- Nom accepté : Tamarindus indica
- Voir sur la TRAMILothèque (davantage d’illustrations)
Sommaire
Noms vernaculaires significatifs TRAMIL
- Cuba, Honduras, Rép. Dominicaine : tamarindo
- Martinique : tamarin
- autres noms créoles : tamaren, tamaren ti fèy
Distribution géographique
Natif d’Afrique tropicale, actuellement cultivée en zones tropicales du monde entier.
Description botanique
Arbre pouvant atteindre 20 m. Feuille paripennées de 5 à 15 cm de long, 10 à 20 paires de folioles oblongues. Inflorescence en racèmes courts pauciflores, axilaires ou terminales, calice en 4 parties, de couleur blanche jaunâtre avec des taches rougâtres. Fleurs à 5 pétales, 2 réduits et 3 grands, oblancéolés, glabres de couleur jaune pâle teintés d’orange ou de rouge. Gousse indéhiscente de 4 à 13 cm de long, de couleur brune claire. Graines indéhiscentes, de 1 à 12, de forme ovales comprimées latéralement, de couleur brune.
Vouchers :
- Jiménez,692,JBSD
- Germosén-Robineau,48,JBSD
- Martínez,4670,ROIG
- Fuentes,4786,ROIG
Emplois traditionnels significatifs TRAMIL
- constipation : pulpe du fruit, jus, voie orale1
- hépatite, ictère : feuille, décoction avec sucre, voie orale2 ; pulpe du fruit mûr, décoction ou macération aqueuse, voie orale2
Recommandations
Selon l’information disponible :
L’emploi contre la constipation, l’hépatite et l’ictère est classé REC basé sur l’usage significatif traditionnel documenté par les enquêtes TRAMIL, les études de toxicité et l’information scientifique publiée.
Ne pas prendre de laxatif ni de purge en cas d’obstruction intestinale ou de douleur abdominale.
Si l’état du patient se détériore, ou que l’hépatite dure plus de 5 jours, la jaunisse ou la constipation plus de 3 jours, consulter un médecin.
L’hépatite et l’ictère étant dangereux pour la santé, il est recommandé de consulter un médecin au préalable. L’emploi de cette ressource doit être considéré comme un complément au traitement médical, sauf contreindication.
A cause des risques documentés d’interaction avec l’aspirine3-4 et l’ibuprophène3, éviter la consommation du fruit qui augmente la biodisponibilité chez les personnes qui prennent ces médicaments, de même que chez les personnes prenant de la chloroquine5 mais cette fois parce qu’il diminue la biodisponibilité.
Ne pas employer avec des femmes enceintes, allaitantes, ni avec des enfants de moins de moins de 5 ans.
Chimie
La plante entière contient de la capsaïcine, pipérine et curcumine6.
La feuille est riche en acides α-oxoglutarique, glyoxylique, oxaloacétique et oxalosuccinique7.
Le fruit contient, outre les acides déjà mentionnés, de l’acide tartarique (8-18%), acétique, citrique, malique et succinique, sucres et pectines (2-3,5%)7-8.
Analyse proximale de 100 g de feuille9: calories : 78; eau : 77,2%; protéines : 5,1%; lipides : 1,0%; glucides : 16,1%; fibres : 1,3%; cendres : 0,6%; calcium : 24 mg; phosphore : 52 mg; fer : 2,0 mg; sodium : 8 mg; potassium : 273 mg; carotène : 2510 μg; thiamine : 0,10 mg; riboflavine : 0,11 mg; niacine : 1,50 mg; acide ascorbique : 6 mg.
Analyse proximale de 100 g de fruit9: calories : 36; eau : 88,9%; protéines : 2,4%; lipides : 0,3%; glucides : 7,6%; fibres : 1%; cendres : 0,8%; calcium : 92 mg; phosphore : 51 mg; fer : 0,6 mg; sodium : 3 mg; potassium : 249 mg; carotène : 312 μg; thiamine : 0,17 mg; riboflavine : 0,21 mg; niacine : 1 mg; acide ascorbique : 31 mg.
Activités biologiques
Travail TRAMIL10
L’extrait aqueux (infusion durant 15 minutes, suivie de macération durant 4 heures) de feuille sèche, in vitro (1 mg de plante sèche/mL), sur hépatocytes isolés de rat, intoxiqués par le ter-butyl hydropéroxyde (TBH) et contre les radicaux libres, modèle de l’inhibition du radical 2,2-diphényl-1-picrylhydrazyl (DPPH), a montré un effet contre la nécrose cellulaire induite par le TBH et une activité antilipopéroxydante.
Travail TRAMIL11
Le jus frais (15% du fruit mûr), (1 et 10 g de matériel végétal/kg), par voie orale à la souris OF-1 mâle (20-25 g), 10 animaux/groupe, modèle de transit intestinal avec charbon actif 10% (0,1 mL/10 g), n’a pas modifié significativement le transit intestinal.
L’extrait méthanolique de fruit in vitro (5,0-10,0 mg/ mL) sur jéjunum isolé de lapin, a eu un effet relaxant statistiquement significatif (p<0,05) mesuré par le blocage des canaux de calcium12.
L’extrait aqueux (33 mL/L) de feuille et tige fraîches, par voie intrapéritonéale au cobaye et l’extrait éthanolique (95%) (3,3 mL/L) sur iléon isolé de cobaye, ont présenté une activité spasmolitique13.
L’extrait aqueux du fruit (60-600 mg/kg) par voie orale à des rongeurs, modèle d’analgésie sur contorsions induites par l’acide acétique, a montré une inhibition dose dépendante. Le même extrait a également augmenté le temps de latence pour l’essai de la plaque chaude. Tous deux de manière statistiquement significative (p<0,05). En conséquence, on lui a reconnu une activité anti nociceptive centrale et périphérique14.
L’extrait aqueux de pulpe du fruit, (100 mg/kg/jour/90 jours), par voie orale au lapin, a réduit la toxicité hépatique provoquée par le fluorure15.
Les extraits aqueux de fruit, feuille (350 mg/kg) et graine non grillée (700 mg/kg), par voie orale au rat (intoxiqué par le paracétamol, 1 g/kg/7 jours) durant 9 jours à partir de la troisième dose de paracétamol, a montré un effet hépatorégénératif statistiquement significatif (p<0,05)16.
Toxicité
Travaux TRAMIL17-19
L’extrait aqueux (décoction à 30%) d’écorce du tronc (rendement : 0,18 mg/mL, 36 mg de solides totaux/ kg), du fruit frais (rendement : 8,08 mg/mL, 1,6 g de solides totaux/kg) et de feuille fraîche (rendement : 1,27 mg/ mL, 254 mg de solides totaux/kg), par voie orale au rat, volume maximum de 2 mL/100 g; équivalent à 6 g de matériel végétal/kg, dose unique sur le modèle de classes toxiques aiguës, n’a provoqué ni mort ni signes de toxicité durant les 14 jours d’observation, ni modifications histopathologiques.
Le fruit administré au poulet Brown Hisex (10% de la ration) a montré une activité hépatotoxique et néphrotoxique des jours 21 à 35 du traitement, qui a persisté partiellement après deux semaines de ration alimentaire normale20.
L’extrait aqueux de feuille sèche (1 mg/plaque) a présenté une activité antihépatotoxique sur culture d’hépatocytes isolés21.
Le fruit, à 2,5% de la ration alimentaire du rat, a inhibé les réactions d’oxydation du foie6.
L’extrait fluide (70%) d’écorce du fruit, modèle in vivo d’induction des micro-noyaux sur moelle osseuse de souris, a montré un effet génotoxique (11,1%)22.
L’extrait aqueux (décoction) de feuille, n’a pas provoqué d’effet génotoxique23.
Le fruit a montré un effet mutagénique sur Salmonella thyphimurium souche TA-1535, mais pas sur les souches 1537, 1538, ni 9824.
L’extrait aqueux (décoction) de feuille, (1820 et 4000 mg/ kg), par voie orale à la souris, modèle de toxicité aiguë, n’a provoqué ni mort ni signes de toxicité25.
L’extrait alcoolique (teinture à 20%) de feuille, en dose unique limite (2000 mg/kg), (4 mL d’extrait sur 3x4 cm de peau durant 24 heures), par voie orale et topique au rat Wistar des deux sexes, n’a provoqué ni mort ni signes de toxicité26.
Le fruit est classé par la « Food and Drug Administration » des USA, dans la catégorie « GRAS » (Generally Regarded As Safe), par voie orale et pour un maximum de 0,81% de la ration alimentaire, ce qui implique qu’il est classé dans la catégorie des substances généralement considérées comme sûres27.
On ne dispose d’aucune information pouvant garantir l’innocuité de ce remède administré aux enfants, aux femmes enceintes ou allaitantes.
Préparation et dosage
Le fruit de Tamarindus indica constitue un aliment de consommation humaine relativement étendue.
Contre l’hépatite ou l’ictère :
Broyer 40-50 grammes de fruit après en avoir enlevé les graines, ajouter ½ litre d’eau bouillie, laisser reposer 12 heures et boire 1 tasse 2 fois par jour.
Ou préparer une décoction avec 30 grammes de feuille dans 4 tasses (1 litre) d’eau, faire bouillir pendant 5 minutes dans un récipient couvert. Laisser refroidir, filtrer et boire 1 tasse 3 fois par jour.
Contre la constipation :
Broyer 40-50 grammes de fruit après en avoir enlevé les graines, liquéfier avec ½ litre d’eau bouillie et boire 1 tasse 1 à 2 fois par jour.
Toute préparation médicinale doit être conservée au froid et utilisée dans les 24 heures.
Références
- LONGUEFOSSE JL, NOSSIN E, 1990-95 Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
- GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984 Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
- GARBA M, YAKASAI IA, BAKARE MT, MUNIR HY, 2003 Effect of Tamarindus indica L. on the bioavailability of ibuprofen in healthy human volunteers. Eur J Drug Metab Pharmacokinet 28(3):179- 184.
- MUSTAPHA A, YAKASAI IA, AGUYE IA, 1996 Effect of Tamarindus indica on the bioavailability of aspirin in healthy human volunteers. Eur J Drug Metab Pharmacokinet 21(3):223-226.
- MAHMOUD BM, ALI HM, HOMEIDA MM, BENNETT JL, 1994 Significant reduction in chloroquine bioavailability following coadministration with the Sudanese beverages Aradaib, Karkabi and Lemon. J Antimicrob Chemother 33(5):1005-1009.
- SAMBAIAH K, SRINIVASAN K, 1989 Influence of spices and spice principles on hepatic mixed function oxigenase system in rats. Indian J Biochem Biophys 26(4):254-258.
- ASWAL BS, BHAKUNI DS, GOEL AK, KAR K, MEHROTRA BN, MUKHERJEE KC, 1984 Screening of Indian plants for biological activity: Part X. Indian J Exp Biol 22(6):312-332.
- WATT JM, BREYER-BRANDWIJK MG, 1962 Medicinal and poisonous plants of Southern and Eastern Africa. Edinburgh & London, UK: 2nd ed. E. & S. Livingstone Ltd., 1457pp.
- DUKE JA, ATCHLEY AA, 1986 Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p156.
- ARVIS PY, JOYEUX M, FLEURENTIN J, MORTIER F, PELT JM, 1986 Influences d’extraits de Cuscuta americana et Tamarindus indicus sur hépatocytes fraîchement isolés de rats. Travail TRAMIL. Laboratoire de pharmacognosie, Centre des Sciences pour l’Environnement, Metz, France.
- MORON FJ, MOREJON Z, VICTORIA MC, BACALLAO Y, FUENTES V, 2009 Acción sobre el tránsito intestinal del zumo fresco del fruto maduro de Tamarindus indica L. (tamarindo) en ratones. Trabajo TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- ALI N, SHAH S, 2010 Spasmolytic activity of fruits of Tamarindus indica L. J Young Pharm 2(3):261-264.
- FENG PC, HAYNES LJ, MAGNUS KE, PLIMMER JR, SHERRATT HS, 1962 Pharmacological screening of some West Indian medicinal plants. J Pharm Pharmacol 14:556-561.
- KHALID S, SHAIK MOSSADEQ WM, ISRAF DA, HASHIM P, REJAB S, SHABERI AM, MOHAMAD AS, ZAKARIA ZA, SULAIMAN MR, 2010 In vivo analgesic effect of aqueous extract of Tamarindus indica L. fruits. Med Princ Pract 19(4):255-259.
- RANJAN R, SWARUP D, PATRA RC, CHANDRA V, 2009 Tamarindus indica L. and Moringa oleifera M. extract administration ameliorates fluoride toxicity in rabbits. Indian J Exp Biol 47(11):900-905.
- PIMPLE BP, KADAM PV, BADGUJAR NS, BAFNA AR, PATIL MJ, 2007 Protective effect of Tamarindus indica Linn against paracetamolinduced hepatotoxicity in rats. Indian J of Pharmaceutical Sciences 69(6):827-831.
- MARTINEZ MJ, MOREJON Z, LOPEZ M, BOUCOURT E, FUENTES V, MORON F, 2005 Clases tóxicas agudas (CTA) de una decocción de corteza del tronco de Tamarindus indica L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- MARTINEZ MJ, MOREJON Z, LOPEZ M, BOUCOURT E FUENTES V, MORON F, 2005 Clases tóxicas agudas (CTA) de decocción de pulpa de fruto fresco de Tamarindus indica L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- MARTINEZ MJ, MOREJON Z, LOPEZ M, BOUCOURT E, FUENTES V, MORON F, 2005 Clases tóxicas agudas (CTA) de una decocción de hoja fresca de Tamarindus indica L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- MOHAMEDAIN KM, MOHAMED OSA, EIBADWI SMA, ADAM SEI, 1996 Effect of feeding Tamarindus indica ripe fruit in brown hisex chicks. Phytother Res 10(7):631-633.
- JOYEUX M, MORTIER F, FLEURENTIN J, 1995 Screening of antiradical, antilipoperoxidant and hepatoprotective effects of nine plant extracts used in Caribbean folk medicine. Phytother Res 9(3):228-230.
- PILOTO FERRER J, VIZOSO A, RAMOS A, GARCIA A, REMIGIO A, VEGA Y, GONZALEZ ML, RODRIGUEZ C, CARBALLO C, 2009 Plantas medicinales. Diez años de evaluaciones toxicogenéticas en el CIDEM. Boletín Latinoamericano y del Caribe de Plantas Medicinales y Aromáticas 8(5):428-434.
- RODRIGUEZ RI, AVILES L, 1995 Evaluación del efecto de las hojas de la especie Tamarindus indica L. sobre la morfología de los espermatozoides. Tesis de Diploma en opción al título de Licenciado en Ciencias Farmacéuticas. Universidad de Oriente, Santiago de Cuba.
- SIVASWAMY SN, BALACHANDRAN B, BALANEHRU S, SIVARAMAKRISHNAN VM, 1991 Mutagenic activity of South Indian food items. Indian J Exp Biol 29(8):730-737.
- PASCUAL JR, 1993 Toxicidad aguda oral de las hojas de Tamarindus indica. Informe de trabajo. Grupo de Toxicología Experimental, Instituto Superior de Ciencias Médicas, Santiago de Cuba. Inédito.
- DEHESA MA, 2005 Contribución al estudio químico farmacéutico de las hojas de la especie Tamarindus indica L. Tesis en opción al grado científico de Doctor en Ciencias Farmacéuticas. Universidad de la Habana, Cuba.
- NATURAL STANDARD, 2011 Tamarind (Tamarindus indica L.). Foods, Herbs & Supplements. http:// naturalstandard.com/index-abstract.asp?create-abstract=flashcardtamarind. asp&title=Tamarind (25dic2011)