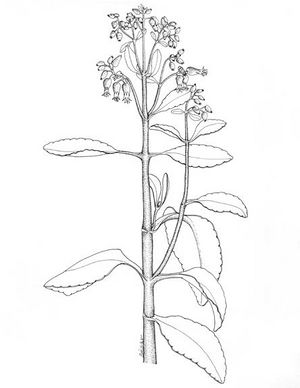
Kalanchoe pinnata (TRAMIL)
| |
- Nom accepté : Kalanchoe pinnata
- Voir sur la TRAMILothèque (davantage d’illustrations)
Sommaire
Noms vernaculaires significatifs TRAMIL
- Costa Rica, Jamaïque : leaf of life
- Guatemala, Honduras : hoja del aire
- Haïti : lou gawou, fey choche
- Martinique : zèb maltèt
- Rép. Dominicaine : bruja
- Ile de San Andrés : tree of life
- autres noms créoles : chans, farin cho, sanglou, tombé lévé, zèb malotèt
Distribution géographique
Originaire de Madagascar, cultivée et naturalisée en Amérique tropicale.
Description botanique
Herbacée succulente, pérenne, glabre, pouvant atteindre 1,5 m. Feuilles souvent pennées-composées, de 10 à 30 cm; folioles oblongues, ovales ou elliptiques, obtuses, crénées; bords avec bourgeons. Panicules de 10 à 40 cm; calice urcéolé, oblong en forme de cloche, de 3 à 3,5 cm; corolle rougeâtre pouvant atteindre 7 cm.
Vouchers :
- Girón,166,CFEH
- Ochoa,274,HPMHV
- Rouzier,42,SOE
- Boulogne,TH12,UAG
- Jiménez,11,JBSD
- Pinzón,21893,CUVC
- Picking,35466,UWI
Emplois traditionnels significatifs TRAMIL
- maux de tête : feuille écrasée, en application sur le front1-5
- rhume : feuille, jus, voie orale6-7 ; feuille fraîche, décoction, voie orale7
- toux : feuille, décoction, voie orale8
- vomissements : feuille, amulette pendue au cou9
Recommandations
L’emploi en amulette contre les vomissements fait partie intégrante du fonds culturel de nos communautés et n’est pas classé dans les catégories définies par TRAMIL.
Selon l’information disponible :
L’emploi contre les maux de tête, le rhume et la toux est classé REC sur la base de l’usage significatif traditionnel documenté par les enquêtes TRAMIL et les études de toxicité.
Si l’état du patient se détériore ou si les maux de tête persistent plus de 2 jours, le rhume ou la toux au-delà de 7 jours, consulter un médecin.
Ne pas employer avec des femmes enceintes ou allaitantes, ni avec des enfants.
Chimie
Travail TRAMIL10
Tamisage phytochimique préliminaire (feuille) :
| alcaloïdes | - |
| flavonoïdes | + |
| quinones | - |
| stéroïdes, terpénoïdes | - |
| saponosides | - |
| comp. phénoliques | + |
| tanins | - |
La partie aérienne contient des flavonoïdes : astragaline, dérivés de quercétine11, camphérol12; des benzénoïdes : acides syringique, 4-hydroxybenzoïque, caféique, p-coumarique et férulique12; des buphadiénolides : 3-acétatebersaldégénine, bryophyline C, bryotoxine B13, 1,3,5,14-tétrahydroxy-19-oxobupha-20,22-diénolide14; des stéroïdes : β-sistostérol, campestérol, entre autres15; des triterpènes : α-amirine16, β-amirine, bryophollénone, bryophollone, bryophynol17; des acides organiques : acétique, citrique, malique, oxalique et succinique18; des alcanes16.
Activités biologiques
L’extrait méthanolique de feuille séchée (100 mg/kg) par voie intrapéritonéale à la souris mâle, modèle de contractions induites par l’acide acétique, a produit un effet analgésique (mais pas sur les modèles de la pression sur la queue), une dépression du système nerveux central et une augmentation du temps de sommeil; avec l’extrait 300 mg/kg, le niveau de GABA (acide gamma-aminobutyrique) a augmenté et une relaxation du muscle squelettique a été observée19.
L’extrait aqueux de feuille séchée (1,6 g/kg), par voie orale au rat, sur le modèle d’œdème de la patte induit par carraghénine, a montré une activité anti-inflammatoire20. Les extraits aqueux et éthanolique de feuille fraîche (0,33 mL/L) sur l’iléon isolé de cobaye, ont présenté des propriétés spasmogènes21.
L’extrait aqueux de feuille, par voie orale au cobaye, n’a pas eu d’effet antitussif22.
Sur une cohorte de 50 patients avec des ulcères trophiques de la jambe, après application locale du jus de la feuille, 46 ont été guéris23.
La plante présente des propriétés cicatrisante et antiseptique. De plus, la tolérance à l’application locale est très bonne, ses effets sont meilleurs que ceux d’Aloe spp24.
On attribue à la bryophilline des propriétés antiseptique25-26; à l’acide coumarique des propriétés bactéricide et à l’acide férulique des propriétés analgésique et antispasmodique27-28.
Toxicité
Travaux TRAMIL29-30
Le jus frais pur (obtenu en écrasant la feuille) et son extrait aqueux (décoction à une concentration de 312,5 mg/mL) de feuille, lyophilisé, ont été administrés par voie orale (0,5 mL/jour/5 jours), à la souris Hsd:ICR (5 mâles et 5 femelles), suivant le modèle OECD 423. Le témoin a été réalisé avec de l’eau distillée et désionisée (0,4 mL) administrée à 10 autres souris de mêmes caractéristiques. La période d’observation a été de 12 jours. Dans les deux cas il n’y a pas eu de mortalité et aucun signe de toxicité n’a été mis en évidence pendant l’expérience ni lors de l’observation ultérieure.
Travail TRAMIL31
Le jus frais pur (obtenu en écrasant la feuille), (1 mL/ jour/5 jours) a été appliqué par voie topique sur une zone de la peau au bas du dos de 10 x 5 cm, abimée par incisions pratiquées au bistouri, à 3 lapins New Zealand, suivant le modèle USP 27 NF22, OECD 404. Le témoin a été réalisé avec de l’eau distillée et déminéralisée sur le côté opposé du traitement des mêmes animaux. La période d’observation a duré 12 jours. Aucun symptôme anormal, ni aucune présence d’érythème ou d’œdème n’a été constaté pendant l’expérience ni lors de l’observation ultérieure.
La plante entière (790 mg/kg) par voie orale au rat, n’a pas montré d’effet toxique32.
L’extrait hydroalcoolique (50%) de plante entière, par voie intrapéritonéale à la souris, a présenté une DL50 = 1 mg/kg33.
L’extrait méthanolique de feuille séchée par voie intrapéritonéale (2400 mg/kg), à la souris mâle, n’a pas produit d’effet toxique général34.
Les extraits aqueux et hydroalcoolique (95%) de tige et de feuille fraîches par voie intrapéritonéale à la souris, ont mis en évidence une dose toxique minimale de 1 mL/animal21.
On a constaté la mort de deux bovins adultes 48 heures après l’ingestion de grandes quantités de plante. Les signes cliniques de l’intoxication ont été l’hypersalivation, l’ataxie, une arythmie cardiaque sévère et une difficulté à respirer. L’autopsie a montré une ruminite (inflammation de l’estomac principal), un rétrécissement bronchique et un emphysème35.
On ne dispose pas d’information garantissant l’innocuité de son emploi sur des enfants, ni avec des femmes enceintes ou allaitantes.
Préparation et dosage
Contre les maux de tête :
Laver soigneusement 2-3 feuilles fraîches, les broyer et appliquer sur le front ou la tête. Couvrir avec un bandage ou un mouchoir. Répéter 4 fois par jour.
Contre le rhume et la toux :
Préparer une décoction avec 15 grammes de feuilles fraîches dans 2 tasses (½ litre) d’eau, faire bouillir 5 minutes dans un récipient couvert. Laisser refroidir, filtrer et boire 1 tasse, 3 fois par jour pendant 3 à 7 jours.
et/ou
Laver soigneusement 5-7 feuilles fraîches, les broyer dans un mortier jusqu’à en exprimer le jus. Boire une cuillère à soupe (15 cc) 3 fois par jour durant 3 à 7 jours.
Toute préparation médicinale doit être conservée au froid et utilisée dans les 24 heures.
Références
- WENIGER B, 1987-88 Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
- GIRON L, 1988 Encuesta TRAMIL (Costa atlántica). Centro Mesoamericano de Tecnología CEMAT, Guatemala, Guatemala.
- LONGUEFOSSE JL, NOSSIN E, 1990-95 Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
- LAGOS-WITTE S, 1988-89, 1996 Encuesta TRAMIL. Laboratorio de Histología Vegetal y Etnobotánica, Departamento de Biología, Universidad Nacional Autónoma de Honduras UNAH, Tegucigalpa, Honduras.
- BOULOGNE I, 2009 Enquête TRAMIL, (Terre-de-Bas et Terre-de-Haut) Les Saintes, UAG, Guadeloupe.
- OCAMPO R, 1988 Encuesta TRAMIL (Costa atlántica), Instituto de Desarrollo Agrario, Universidad de Costa Rica, San José, Costa Rica.
- PICKING D, MITCHELL S, DELGODA R, YOUNGER N, 2011 TRAMIL survey. Natural Products Institute, The Biotechnology Centre & Tropical Metabolic Research Institute, University of the West Indies, Mona, Jamaica.
- PINZON M, 1994 Encuesta TRAMIL (Isla de San Andrés). Laboratorio de Fitofarmacología, Departamento de Farmacología, Facultad de Salud, Universidad del Valle, Cali, Colombia.
- WENIGER B, ROUZIER M, 1986 Enquête TRAMIL. Service Oecuménique d’Entraide SOE, Port au Prince, Haïti.
- WENIGER B, SAVARY H, DAGUIHL R, 1984 Tri phytochimique de plantes de la liste TRAMIL. Laboratoire de chimie des substances naturelles, Faculté de Médecine et de Pharmacie, Université d’Etat d’Haïti, Port au Prince, Haïti.
- GAIND KN, GUPTA RL, 1971 Flavonoid glycosides from Kalanchoe pinnata. Planta Med 20(4):368- 373.
- GAIND KN, GUPTA RL, 1973 Phenolic components from the leaves of Kalanchoe pinnata. Planta Med 23(12):149-153.
- YAMAGISHI T, YAN X, WU R, MC PHAIL D, MC PHAIL A, LEE K, 1988 Structure and stereochemistry of bryophyllin-A, a novel potent cytotoxic bufadienolide orthoacetate from Bryophyllum pinnatum. Chem Pharm Bull 36(4):1615-1617.
- YAN XZ, LEE KS, YAMAGISHI T, 1992 Isolation and identification of cytotoxic components from Bryophyllum pinnatum. Shanghai Yike Daxue Xuebao 19(3):206-208.
- AKIHISA T, KOKKE W, TAMURA T, MATSUMOTO T, 1991 Sterols of Kalanchoe pinnata: first report of the isolation of both C-24 epimers of 24-alkyl-delta-25-sterols from a higher plant. Lipids 26(8):660-665.
- GAIND KN, GUPTA RL, 1972 Alkanes, alkanols, triterpenes and sterols from Kalanchoe pinnata. Phytochemistry 11(4):1500-1502.
- SIDDIQUI S, FAIZI S, SIDDIQUI B, SULTANA N, 1989 Triterpenoids and phenanthrenes from leaves of Bryophyllum pinnatum. Phytochemistry 28(9):2433-2438.
- BULEN WA, VARNER JE, BURRELL RC, 1952 Separation of organic acids from plant tissues. Anal Chem 24:187-190.
- PAL S, SEN T, CHAUDHURI AK, 1999 Neuropsychopharmacological profile of the methanolic fraction of Bryophyllum pinnatum leaf extract. J Pharm Pharmacol 51(3):313-318.
- HEMA D, TIDJANI M, BASSENE E, POUSSET JL, GIONO-BARBER H, 1986 African medicinal plants. XXIV. Study of the antiinflammatory activity of Bryophyllum pinnatum. Plant Med Phytother 20(3):231-235.
- FENG PC, HAYNES L, MAGNUS K, PLIMMER J, SHERRATT H, 1962 Pharmacological screening of some West Indian medicinal plants. J Pharm Pharmacol 14(1):556-561.
- ANDRONOVA L, 1972 Antitussive properties of certain medical plants. Rast Resur 8:588-591.
- BERSHTEJN E, 1972 Utilisation du jus de Kalanchoe pinnata dans le traitement des ulcères trophiques de la jambe. Vest Khir URSS 108(3):116-118.
- SVANIDZE N, LANOVENKLY V, SÁNCHEZ A, RODRÍGUEZ P, 1975 Kalanchoe pinnata como planta medicinal en Cuba. Rev Cub Farm 9(3):225-228.
- BOAKYE-YIADOM K, 1977 Antimicrobial properties of some West African medicinal plants. 1. Antimicrobial action of Bryophyllum pinnatum. Quart J Crude Res 15(4):201-202.
- PERRY LM, METZGER J, 1980 Medicinal plants of East and Southeast Asia: attributed properties and uses. Cambridge, USA: MIT Press.
- DUKE JA, 1992 Handbook of biologically active phytochemicals and their bioactivities. Boca Raton, USA: CRC Press.
- DUKE JA, 1992 Handbook of phytochemical constituents of GRAS Herbs and other economic plants. Boca Raton, USA: CRC Press.
- PAZOS L, COTO T, GONZALEZ S, 2003 Toxicidad oral, aguda en ratones, de la hoja de Kalanchoe pinnata. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
- PAZOS L, COTO T, GONZALEZ S, 2003 Toxicidad oral, aguda en ratones, del extracto acuoso del zumo de la hoja de Kalanchoe pinnata. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
- PAZOS L, COTO T, GONZALEZ S, 2003 Estudio de irritabilidad dérmica, en piel lesionada de conejo, de hoja fresca machacada de Kalanchoe pinnata. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
- YOKEL R, OGZEWALLA CD, 1981 Effects of plant ingestion in rats determined by the conditioned taste aversion procedure. Toxicon 19(2):223-232.
- BHAKUNI O, DHAR ML, DHAR MM, DHAWAN BN, MEHROTRA BN, 1969 Screening of Indian plants for biological activity. Part II. Indian J Exp Biol 7(4):250-262.
- PAL S, SEN T, CHAUDHURI AKN,1999 Neuropsychopharmacological profile of the methanolic fraction of Bryophyllum pinnatum leaf extract. J Pharm Pharmacol 51(3):313-318.
- REPPAS GP, 1995 Bryophyllum pinnatum poisoning of cattle. Aust Vet J 72(11):425-427