Foeniculum vulgare (TRAMIL) : Différence entre versions
| Ligne 7 : | Ligne 7 : | ||
|nomcourtsuivant=''Gliricidia sepium'' | |nomcourtsuivant=''Gliricidia sepium'' | ||
}} | }} | ||
| + | [[File:Foeniculum vulgare plante TRAMIL.jpg|thumb]] | ||
| + | [[File:Foeniculum vulgare fleurs TRAMIL.jpg|thumb]] | ||
| + | [[File:Foeniculum vulgare dessin TRAMIL.jpg|thumb]] | ||
Version actuelle en date du 13 novembre 2020 à 19:22
| |
- Nom accepté : Foeniculum vulgare
- Voir sur la TRAMILothèque (davantage d’illustrations)
Sommaire
Noms vernaculaires significatifs TRAMIL
- Haïti : anni
- Rép. Dominicaine : hinojo (en RD et à Cuba, le nom vernaculaire « hinojo » désigne indistinctement Anethum graveolens et F. vulgare)
- autres noms créoles : fenouy, lanni
Distribution géographique
Originaire de la région méditerranéenne, cultivée et fréquemment naturalisée dans les régions tempérées et subtropicales du monde.
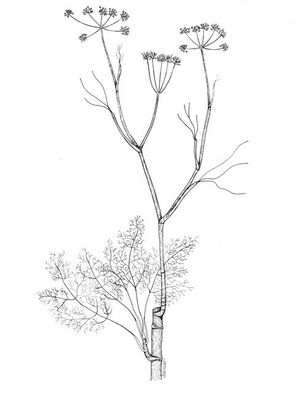
Description botanique
Herbacée dressée pérenne, glabre, habituellement très ramifiée. Feuilles alternes, ovées à triangulaires, pouvant atteindre 30 cm, pennati-composées, avec divisions filiformes. Inflorescence en ombelles avec de nombreuses fleurs, pouvant atteindre 12 cm de diamètre; pétales jaunes. Fruit oblong, glabre, légèrement comprimé, avec côtes aiguës et égales.
Cette espèce est fréquemment confondue avec Anethum graveolens, laquelle a une gousse pétiolaire plus courte et les 2 côtes latérales du fruit plus amples.
Vouchers : Jiménez,688,JBSD Martínez,4623,ROIG
Emplois traditionnels significatifs TRAMIL
- douleurs d’estomac, douleurs abdominales, flatulences : graine et/ou feuille, décoction, voie orale1
- douleurs d’oreille : feuille, jus, gouttes (instillation) dans l’oreille2
Recommandations
Selon l’information disponible :
L’emploi contre les douleurs d’estomac, les douleurs abdominales et les flatulences est classé REC sur la base de l’usage significatif traditionnel documenté par les enquêtes TRAMIL, les études de validation, de toxicité et l’information scientifique publiée.
Si l’état du patient se détériore ou si les douleurs d’estomac persistent au-delà de 3 jours, consulter un médecin. L’emploi contre les douleurs d’oreille est classé REC sur la base de l’usage significatif traditionnel documenté par les enquêtes TRAMIL et les études de toxicité.
Les douleurs d’oreille risquant d’être dues à une otite moyenne ou interne, on recommande de consulter un médecin au préalable. Son utilisation est contre-indiquée en présence de sécrétions dans l’oreille et/ou d’une éventuelle perforation du tympan.
Toute application dans l’oreille doit se conformer aux plus strictes mesures d’hygiène, pour empêcher la contamination ou une infection surajoutée.
Si l’état du patient se détériore ou si les douleurs d’oreille durent plus de 2 jours, consulter un médecin.
Ne pas employer avec des enfants de moins de 3 ans, ni avec des femmes enceintes ou allaitantes.
La graine peut provoquer des réactions d’hypersensibilité.
Chimie
Le fruit et les parties aériennes ont été amplement étudiés et contiennent, entre autres composants, de l’huile essentielle, constituée principalement par : trans et cisanéthol (68%), limonène, fenchone3. Le fruit contient des flavonoïdes : féniculine, juglanine, camphérol, quercétine et dérivés, iso-quercitrine, rutine4; des alcaloïdes : acétylcholine (74 nmoles/g), choline (2674 nmoles/g)5; des coumarines : psoralène, xanthotoxine6, méthoxypsoralène, iso-pimpinelline7, scoparone et séséline8.
La feuille contient des flavonoïdes : kaempférol, quercétine, iso-quercitrine9, cinnaroside10 et guayavérine11.
Analyse proximale pour 100 g de feuille12: calories : 28; eau : 90%; protéines : 2,8%; lipides : 0,4%; glucides : 5,1%; fibres : 0,5%; cendres : 1,7%; calcium : 100 mg; phosphore : 51 mg; fer : 2,7 mg; potassium : 397 mg; carotène : 2100 μg; acide ascorbique : 31 mg.
Analyse proximale pour 100 g de graine12: calories : 345; eau : 8,8%; protéines : 15,8%; lipides : 14,9%; glucides : 52,3%; fibres : 15,7%; cendres : 8,2%; calcium : 1196 mg; phosphore : 487 mg; fer : 18,5 mg; sodium : 8,8 mg; potassium : 1694 mg; carotène : 81 μg; thiamine : 0,41 mg; riboflavine : 0,35 mg; niacine : 6,05 mg.
Activités biologiques
Travail TRAMIL13
L’extrait aqueux (décoction) de feuille fraîche (15-25 g/L) et l’infusion de graine séchée (5-10 g/L), par voie orale à l’être humain adulte (120-240 mL), employées en phytothérapie clinique, ont eu des résultats positifs lors du contrôle de symptômes spasmodiques mineurs du tube digestif.
L’extrait aqueux (10%) de graine séchée a stimulé le muscle lisse du jéjunum de rat et le muscle strié du rectus abdominus de grenouille5.
L’extrait acétonique de graine, administré par voie orale au rat pendant 10-15 jours, a engendré des effets oestrogéniques14.
L’extrait éthanolique (80%) de fruit séché (100 mg/kg), par voie orale au rat, modèle d’inflammation de patte induite par carraghénnine, a inhibé dans une proportion de 36% l’oedème expérimental15.
Le fruit séché a présenté une action carminative, aromatique, anti-inflammatoire, antimicrobienne, diurétique et stimulante de l’appétit16.
On attribue à l’huile essentielle des propriétés eupeptiques, carminatives et antiseptiques16-17.
On considère que l’anéthol et ses deux polymères : dianéthol et photoanéthol, sont des agents oestrogéniques actifs18. Dans la Pharmacopée Soviétique, elle figurait comme stimulant de la digestion et comme expectorant19.
Toxicité
Travail TRAMIL20
Le jus lyophilisé de feuille (500 g), en application topique (0,5 mL et 0,75 mL) sur la peau rasée de 16 cobayes blancs Hantley, répartis en deux groupes équivalents des deux sexes (450-500 g) n’a pas provoqué d’irritation dermique (indice d’irritation primaire inférieure à 5), 24 et 72 heures après l’application. Les analyses histopathologiques n’ont pas montré d’altérations.
Travail TRAMIL21
Le jus de feuille fraîche pilée et exprimée avec une gaze, (patch avec 0,6 mL/6 cm2 de peau/4 heures) par voie topique sur 3 lapins albinos New Zealand, modèle d’irritabilité dermique aigüe de Draize. Le patch a été retiré au bout de 4 heures et la zone a été lavée. Les lectures à la recherche d’érythème et d’oedème après 1, 24, 48 et 72 heures, ont montré un indice de 0,00 qui classifie le jus comme non irritant.
Travail TRAMIL13
L’extrait aqueux (décoction) de feuille fraîche (15-25 g/L) et l’infusion de graine séchée (5-10 g/L), administrées jusqu’à 500 mL/jour/personne, ont présenté un goût anisé aromatique et n’ont pas produit de manifestations objectives ni subjectives d’effets indésirables sur les patients.
Travail TRAMIL22
L’extrait aqueux (décoction à 30%) de feuille fraîche (rendement : 0,97 mg/mL), en dose unique (volume maximum de 2 mL/100 g; équivalent à 6 g de matériel végétal/kg ou 194 mg de solides totaux/kg), par voie orale au rat, modèle de classes toxiques aigües, n’a pas entraîné de mort ni de signes évidents de toxicité pendant les 14 jours d’observation, ni de changement histologique.
L’extrait éthanolique (95%) de parties aériennes (100 mg/ jour), administré par voie orale à la souris femelle a entraîné la mort; chez le mâle cette dose s’est révélée non toxique. L’extrait alcoolique de la plante, jusqu’à 3 g/kg, n’a pas été spermicide23.
L’extrait méthanolique (80%) de parties aériennes fraîches (2 g/kg), par voie orale à la souris, n’a pas entraîné de mort ni de signes évidents de toxicité24.
Les préparations avec des doses de plante élevées peuvent donner des convulsions16.
L’exposition répétée de la peau à la graine peut provoquer une dermatite allergique chez des individus prédisposés25.
On ne dispose pas d’information garantissant l’innocuité de son emploi médicinal avec des enfants, ni avec des femmes enceintes ou allaitantes.
Préparation et dosage
La feuille de Foeniculum vulgare constitue un aliment de consommation humaine relativement répandue et la graine, une source industrielle d’huile essentielle.
Contre les douleurs d’estomac, les douleurs abdominales ou les flatulences :
Préparer une décoction avec 0,3-0,6 grammes de graines séchées ou 3-5 grammes de feuilles fraîches dans 1 tasse (250 mL) d’eau, faire bouillir 10 minutes dans un récipient couvert. Filtrer, laisser refroidir et boire 1 tasse 3 fois par jour26-27.
Contre les douleurs d’oreille :
Laver soigneusement les feuilles, les écraser et instiller 2 gouttes du jus obtenu dans l’oreille affectée 2 ou 3 fois par jour.
Toute préparation médicinale doit être conservée au froid et utilisée dans les 24 heures.
Références
- GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984 Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
- WENIGER B, ROUZIER M, 1986 Enquête TRAMIL. Service Oecuménique d’Entraide SOE, Port au Prince, Haïti.
- HAGINIWA J, HARADA M, MORISHITA I, 1963 Pharmacological studies on crude drugs. VII. Properties of essential oil components of aromatics & their pharmacological effect on mouse intestine. Yakugaku Zasshi 83:624.
- AKUNZEMANN J, HERRMANN K, 1977 Isolation and identification of flavon(ol)-O-glycosides in caraway (Carum carvi L.), fennel (Foeniculum vulgare Mill.), anise (Pimpinella anisum L.), and coriander (Coriandrum sativum L.), and of flavone-Cglycosides in anise. I. Phenolics of spices. Z Lebensm Unters Forsch 164:194-200.
- HARANATH P, AKTHER M, SHARIF S, 1987 Acetylcholine and choline in common spices. Phytother Res 1(2):91-92.
- ZOBEL A, BROWN S, 1991 Psoralens on the surface of seeds of Rutaceae and fruits of Umbelliferae and Leguminosae. Can J Bot 69(3):485-488.
- CESKA O, CHAUDHARY S, WARRINGTON P, ASHWOOD-SMITH M, 1987 Photoactive furocoumarins in fruits of some Umbellifers. Phytochemistry 26(1):165-169.
- MENDEZ J, CASTRO-POCEIRO J, 1981 Coumarins in Foeniculum vulgare fruits. Rev Latinoamer Quim 12(2):91- 92.
- SALEH N, EL-NEGOUMY S, EL-HADIDI M, HOSNI H, 1983 Comparative study of the flavonoids of some local members of the Umbelliferae. Phytochemistry 22(6):1417-1420.
- LATTANZIO V, MARCHESINI A, 1981 Determination of plant phenols by gel filtration. J Food Sci 46(6):1907- 1909.
- HARBONE J, BOARDLEY M, 1984 Use of high-performance liquid chromatography in the separation of flavonol glycosides and flavonol sulphates. J Chromatogr 299(2):377- 385.
- DUKE JA, ATCHLEY AA, 1986 Handbook of proximate analysis tables of higher plants. Boca Ratón, USA: CRC Press. p75.
- CARBALLO A, 1995 Plantas medicinales del Escambray cubano. Informe TRAMIL. Laboratorio provincial de producción de medicamentos, Sancti Spiritus, Cuba.
- MALINI T, VANITHAKUMARI G, MEGALA N, ANUSYA S, DEVI K, ELANGO V, 1985 Effect of Foeniculum vulgare Mill. seed extract on the genital organs of male and female rats. Indian J Physiol Pharmacol 29(1):21-26.
- MASCOLO N, AUTORE G, CAPASSO F, MENGHINI A, FASULO MP, 1987 Biological screening of Italian medicinal plants for anti-inflammatory activity. Phytother Res 1(1):28-31.
- DUKE JA, 1988 Handbook of medicinal herbs. Boca Raton, USA: CRC Press.
- PINKAS M, BEZANGER-BEAUQUESNE L, 1986 Les plantes dans la thérapeutique moderne. Paris, France: 2 éd. Ed. Maloine.
- ALBERT PULEO M, 1980 Fennel and anise as estrogenic agents. J Ethnopharmacol 2(4):337-344.
- HURTADO M, CARBALLO A, 1990 Las plantas medicinales TRAMIL en la farmacopea soviética. Centro de Investigaciones de Fitoterapia y Medicina Tradicional, Topes de Collantes, Cuba.
- ALFONSO H, 1992 Evaluación de la toxicidad dérmica de Momordica charantia L., Foeniculum vulgare Mill y Cassia occidentalis L. en cobayos. Informe TRAMIL. Centro Nacional de Salud Animal CENSA, La Habana, Cuba.
- MARTINEZ MJ, LOPEZ M, MOREJON Z, BOUCOURT E, FUENTES V, MORON F, 2007 Irritabilidad dérmica primaria del zumo de hojas frescas machacadas y exprimidas mediante gasa de Foeniculum vulgaris Mill. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- MARTINEZ MJ, MOREJON Z, LOPEZ M, BOUCOURT E, FUENTES V, MORON F, 2005 Clases tóxicas agudas (CTA) de una decocción de hoja fresca de Foeniculum vulgare Miller. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
- SHAH A, QURESHI S, AGEEL A, 1991 Toxicity studies in mice of ethanol extracts of Foeniculum vulgare fruit and Ruta chalepensis aerial parts. J Ethnopharmacol 34(2/3):167-172.
- HUSSAIN RA, POVEDA LJ, PEZZUTO JM, SOEJARTO DD, KINGHORN AD, 1990 Sweetening agents of plant origin: phenylpropanoid constituents of seven sweet-tasting plants. Econ Bot 44(2):174-182.
- SEETHARAM K, PASRICHA J, 1987 Condiments and contact dermatitis of the finger-tips. Indian J Dermatol Venereol Leprol 53(6):325-328.
- ASSOCIATION SCIENTIFIC COMMITTEE, 1983 British herbal pharmacopoeia. Bournemouth, England: British Herbal Medicine Association.
- CARBALLO A, 1995 Cálculo de concentración y dosis de las drogas vegetales TRAMIL: Mensuraciones farmacognósticas y aproximaciones técnico-clínicas. Laboratorio provincial de producción de medicamentos, Sancti Spiritus, Cuba.