Cryptolepis sanguinolenta (PROTA)
Introduction |
| Importance générale | |
| Répartition en Afrique | |
| Répartition mondiale | |
| Légume | |
| Colorant / tanin | |
| Médicinal | |
| Fibre | |
| Sécurité alimentaire | |
Cryptolepis sanguinolenta (Lindl.) Schltr.
- Protologue: Westafr. Kautschuk-Exped. 308 (1900).
- Famille: Asclepiadaceae (APG: Apocynaceae)
- Nombre de chromosomes: 2n = 22
Origine et répartition géographique
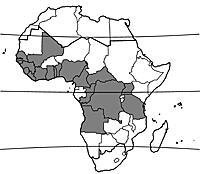
Cryptolepis sanguinolenta se rencontre depuis le Sénégal jusqu’au Nigeria, et on l’a signalé également au Cameroun, en Centrafrique, au Congo, en R.D. du Congo, en Ouganda, en Tanzanie et en Angola.
Usages
Les racines de Cryptolepis sanguinolenta fournissent une teinture jaune employée pour colorer le cuir, par ex. les peaux de chèvre tannées en Côte d’Ivoire et au Nigeria. On pile les racines dans un mortier en bois, on ajoute un peu d’eau chaude et on agite le mélange, qui a une couleur jaune terne et doit être utilisé immédiatement. La peau de chèvre tannée est tout d’abord traitée avec de l’huile d’arachide, et ensuite plongée dans le bain de teinture, en frottant bien l’extrait sur la surface pour le faire pénétrer. Après quelques minutes, on ajoute un morceau de pâte préparée avec du tamarin (Tamarindus indica L.). Cette pâte, préparée à partir des graines et de la pulpe des fruits, est trempée dans de l’eau froide que l’on chauffe progressivement jusqu’à obtenir une masse pulpeuse. Ce nouveau mélange est également frotté sur la peau. Celle-ci est exposée à l’air pendant 2–3 minutes, puis à nouveau frottée avec le mélange pendant environ 5 minutes, bien essuyée et pendue pour la sécher. La pâte de tamarin a pour effet de purifier la couleur car elle élimine la teinte rouge qui pourrait résulter de l’addition d’alcali dans le bain de teinture.
La médecine traditionnelle emploie les racines amères à des fins diverses. Les racines sont mâchées tandis que l’écorce de racine ou des extraits de racine se prennent pour traiter la fièvre, l’hépatite (Guinée-Bissau), le paludisme (Ghana), l’hypertension et les infections des voies urinaires et des voies respiratoires supérieures (Ghana, Nigeria), les coliques, les maux d’estomac, la dysenterie amibienne et la diarrhée (Sénégal, Ghana, Nigeria, R.D. du Congo, Ouganda), les blessures, la rougeole, les hernies, les morsures de serpent (Ouganda), les rhumatismes (Sénégal, Nigeria), l’insomnie (Ghana) et comme tonique (Sénégal, Nigeria).
Au Burkina Faso, les feuilles sont utilisées comme légume. En Ouganda, la tige est employée en tant que corde dans la construction des maisons.
Production et commerce international
Les racines de Cryptolepis sanguinolenta sont récoltées dans la nature et vendues sur les marchés locaux d’Afrique de l’Ouest à des fins médicinales et pour l’extraction du colorant. Certains antipaludéens ont été mis au point, comme par exemple “Phytolaria” au Ghana et “Malaria’” au Mali. La plante crue en poudre et l’extrait aqueux lyophilisé ont également été formulés en comprimés et en suppositoires.
Propriétés
Les feuilles et les racines de Cryptolepis sanguinolenta sont riches en alcaloïdes indoliques bioactifs tels que la cryptolépine, qui est le principal constituant de l’écorce de racine et le premier alcaloïde isolé de la plante. On a isolé des racines une série d’alcaloïdes de structure voisine tels que hydroxycryptolépine, isocryptolépine, cryptospirolépine, néocryptolépine, néocryptine et quindoline. Dans un extrait aqueux des racines, seule la cryptolépine était détectée, et elle constitue la principale ou la seule source de colorant jaune dans les bains de teinture. D’autres teintures alcaloïdes jaunes telles que la berbérine extraite de Berberis et Mahonia spp. ont eu une importance historique en Asie, en Europe et en Amérique.
La cryptolépine est l’alcaloïde de cette plante qui a fait l’objet des recherches les plus poussées, et elle a une activité antiplasmodium, anticancéreuse, antifongique, antibactérienne, hypotensive, antipyrétique, anti-inflammatoire et anti-hyperglycémique. Mais c’est son activité antipaludéenne qui a été la plus étudiée. La cryptolépine a une puissante activité antiplasmodium in vitro, mais elle a également de considérables propriétés cytotoxiques, génotoxiques, intercalantes de l’ADN et inhibitrices de la topoïsomérase II. Mais lors d’une précédente étude, il a été démontré que l’action antiplasmodium de la cryptolépine était due, au moins en partie, à une action analogue à celle de la chloroquine, qui ne dépend pas de l’intercalation dans l’ADN. La synthèse d’une série d’analogues de la cryptolépine a été signalée, et il a été montré que certains d’entre eux avait une activité antiplasmodium plus élevée in vitro contre des souches de Plasmodium falciparum aussi bien sensibles à la chloroquine que résistantes. Par ailleurs, on a découvert que plusieurs composés avaient une activité antiplasmodium significative chez des souris infectées avec Plasmodium berghei, et, fait important, contrairement à la cryptolépine, aucune toxicité apparente n’a été constatée chez les souris. Ces résultats indiquent que les analogues de la cryptolépine ont un potentiel comme composés de base pour de nouveaux agents antipaludéens. Plusieurs dérivés de néocryptolépine ont été évalués afin d’y déceler une éventuelle activité contre des souches de Plasmodium falciparum aussi bien sensibles que résistantes à la chloroquine. Leur activité contre Trypanosoma brucei et Trypanosoma cruzi, ainsi que leur cytotoxicité sur des cellules humaines a été analysée. Ces molécules ont manifesté une activité antiplasmodium plus élevée que les composés de départ et une cytotoxicité plus faible. Dans un autre essai, la cryptolépine et 8 analogues synthétiques ont été analysés afin de déceler une éventuelle activité in vitro contre Trypanosoma brucei : 4 composés se sont révélés extrêmement puissants. Lorsque les tests ont porté sur des rats, le composé le plus efficace découvert a été la 2,7-dibromocryptolépine.
L’hydrochlorure de cryptolépine a manifesté une activité significative contre la bactérie à croissance rapide Mycobacterium fortuitum, dont on a récemment montré l’utilité dans l’évaluation de médicaments antituberculeux. Une activité a été également observée contre 5 autres Mycobacterium spp. Plusieurs analogues de la cryptolépine se sont avérés plus efficaces que la cryptolépine contre Candida albicans, Cryptococcus neoformans et Aspergillus niger. La comparaison de plusieurs de ces analogues avec des agents antifongiques de référence a montré qu’ils étaient aussi puissants que les médicaments antifongiques classiques. Un extrait à l’éthanol d’écorce de racine a révélé une puissante activité antibactérienne et une activité antivirale modérée. Les composés isolés (cryptolépine, hydroxycryptolépine, néocryptolépine, biscryptolépine et quindoline) ont fortement inhibé la croissance de bactéries gram-positives et montré une activité modérée ou nulle contre des bactéries gram-négatives sélectionnées. Ils ont également eu un effet bactéricide qui dépend de la souche bactérienne. On a découvert que la cryptolépine avait une activité modérée contre le virus Herpes simplex. L’activité antibactérienne de la néocryptolépine et de la biscryptolépine était davantage bactériostatique que bactéricide. Il n’a pas été observé d’activité antifongique des alcaloïdes contre Epidermophyton floccosum, Trichophyton rubrum et Aspergillus fumigatus. Les concentrations inhibitrices minimales de cryptolépine, ainsi que des extraits éthanoliques et aqueux de racines ont été établies pour 65 souches de Campylobacter jejuni, 41 souches de Campylobacter coli et 86 souches de Vibrio cholerae. L’activité de l’extrait à l’éthanol contre les souches de Campylobacter est plus élevée que celle des médicaments commerciaux. L’extrait à l’éthanol et la cryptolépine ont manifesté une certaine activité contre des souches de Vibrio cholerae.
La cryptolépine fait chuter le taux de glucose de façon significative lorsqu’elle est administrée par voie orale dans un modèle avec des souris de diabète de type 2. L’effet antihyperglycémique de la cryptolépine conduit à une importante baisse de la concentration d’insuline dans le plasma, et s’accompagne d’un renforcement manifeste de l’élimination du glucose régulée par l’insuline.
La cryptolépine a réduit les contractions de l’iléon isolé de cobaye induites par l’acétylcholine ou la prostaglandine E2. Elle a également diminué la réponse réflexe de l’iléon provoquée par stimulation électrique coaxiale. D’autres études ont confirmé l’activité anticholinergique de la cryptolépine.
De plus, un extrait aqueux de racine a eu des effets anxiogènes, mais également anxiolytiques lors de différents essais sur des souris. L’extrait a diminué l’activité locomotrice spontanée chez des souris et a prolongé la durée de sommeil au pentobarbitone, mais dans une autre étude, il a induit un comportement anxiogène. Une explication plausible est que les effets sédatifs et quasi-anxiogènes observés relèvent de mécanismes différents sur des récepteurs différents.
Il a été démontré que l’hydroxycryptolépine inhibait l’oxydase de xanthine et agissait comme piégeur des anions superoxydes.
Une étude sur l’impact des facteurs environnementaux sur la teneur totale en alcaloïdes de différentes parties végétales de Cryptolepis sanguinolenta de diverses provenances ghanéennes a montré qu’elle était influencée par les fluctuations en température, précipitations, humidité relative et durée d’ensoleillement.
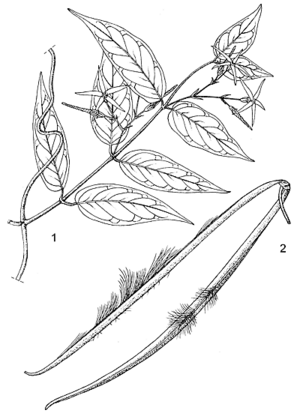
Description
- Arbuste volubile et grimpant à fines branches atteignant 8 m de long, contenant un jus jaune orangé virant au rouge au séchage.
- Feuilles opposées, simples et entières, glabres ; stipules absentes ; pétiole de 1–1,5 cm de long ; limbe elliptique à ovale, de 2,5–10 cm × 1–6 cm, base arrondie à cunéiforme, apex acuminé.
- Inflorescence : cyme axillaire atteignant 8 cm de long, pauciflore, lâche.
- Fleurs bisexuées, régulières, 5-mères, d’environ 1,5 cm de long, jaune verdâtre ; pédicelle de 0,5–1,5 cm de long ; sépales lancéolés, aigus ; corolle à tube d’environ 5 mm de long, lobes disposés en étoile, lancéolés, d’environ 12 mm de long, contortés vers la gauche dans le bouton floral.
- Fruit : paire de follicules étalés, chacun étroitement cylindrique, atteignant 18 cm × 0,5 cm.
- Graines d’environ 12 mm de long, portant une touffe de longs poils soyeux.
Autres données botaniques
Le genre Cryptolepis est classé dans la sous-famille Periplocoideae. Il comprend une trentaine d’espèces en Afrique, en Asie et en Australie. La majorité des espèces se rencontrent en Afrique de l’Est et à Socotra (Yémen). La répartition et la composition chimique de Cryptolepis sanguinolenta sont très différentes de celles des autres espèces africaines de Cryptolepis. Les feuilles de la plupart des espèces de Cryptolepis contiennent des composés phénoliques, qui sont absents des feuilles de Cryptolepis sanguinolenta. Toutefois, les feuilles de Cryptolepis sanguinolenta contiennent des alcaloïdes qui sont rares chez d’autres espèces de Cryptolepis.
Une autre espèce de Cryptolepis présente dans la région a des usages médicinaux. Cryptolepis eburnea (Pichon) Venter se rencontre dans la région des forêts d’Afrique de l’Ouest. En Sierra Leone, le latex de l’écorce est appliqué sur la peau pour traiter le craw-craw (l’onchocercose).
Ecologie
Cryptolepis sanguinolenta se rencontre dans les savanes, les forêts sèches et les forêts galeries, généralement près de l’eau, depuis le niveau de la mer jusqu’à 850 m d’altitude.
Multiplication et plantation
Les graines de Cryptolepis sanguinolenta perdent rapidement leur viabilité ; cependant, les graines fraîchement récoltées présentent une germination de 90–100%. On peut cultiver les semis en sachet de polyéthylène et les repiquer au début de la saison des pluies. Les plantes fleurissent 10 mois après le semis.
La viabilité des graines a été testée dans trois types de conditions de conservation différents : à température ambiante (25–28ºC), au réfrigérateur (10–12ºC) et au congélateur (-18– -21ºC), en prenant comme conteneurs une boîte en papier, un bocal en verre, des sachets plastiques ordinaires ou noirs. Les résultats ont indiqué qu’aucun de ces conteneurs n’était capable d’empêcher la perte progressive de viabilité des graines, mais c’est le sac en polyéthylène ordinaire qui a donné les meilleurs résultats. Pendant les 4 premières semaines, la viabilité était meilleure à température ambiante, et à 12 semaines elle était supérieure au réfrigérateur.
Ressources génétiques
Cryptolepis sanguinolenta est répandu et ne semble pas menacé d’érosion génétique. Au Ghana, des essais de multiplication in vitro de jeunes plants et une conservation à croissance lente ont donné des résultats positifs comme moyen de conservation de la diversité génétique.
Perspectives
Cryptolepis sanguinolenta a beaucoup intéressé les chercheurs au cours des années passées, surtout en raison des intéressantes activités antipaludéennes et anticancéreuses de la cryptolépine, l’alcaloïde le plus important isolé surtout des racines, ainsi que les activités encore plus puissantes de tout un éventail d’analogues de la cryptolépine, qui ont une cytotoxicité inférieure. Des extraits de racines et divers alcaloïdes isolés ont également montré diverses activités significatives contre toutes sortes de bactéries et de champignons, confirmant ainsi son usage en médecine traditionnelle. Mais un approfondissement des recherches est toutefois nécessaire afin d’évaluer le potentiel de ces alcaloïdes et de déterminer les risques pour la santé de son usage en médecine traditionnelle. Cryptolepis sanguinolenta restera localement important comme source de teinture jaune.
Références principales
- Ameyaw, Y., Akotoye, H.K. & Boahen, Y.O., 2007. The effect of environmental factors on the total alkaloid contents of Cryptolepis sanguinolenta (Lindl.) Schtr. International Journal of Chemical Sciences 5(2): 462–476.
- Ansah, C., Mfoafo, E.A., Woode, E., Opoku-Okrah, C., Owiredu, W.K.B.A. & Duwiejua, M., 2008. Toxicological evaluation of the anti-malarial herb Cryptolepis sanguinolenta in rodents. Journal of Pharmacology and Toxicology 3(5): 335–343.
- Berhaut, J., 1971. Flore illustrée du Sénégal. Dicotylédones. Volume 1. Acanthacées à Avicenniacées. Gouvernement du Sénégal, Ministère du Développement Rural et de l’Hydraulique, Direction des Eaux et Forêts, Dakar, Senegal. 626 pp.
- Burkill, H.M., 1997. The useful plants of West Tropical Africa. 2nd Edition. Volume 4, Families M–R. Royal Botanic Gardens, Kew, Richmond, United Kingdom. 969 pp.
- Dalziel, J.M., 1926. African leather dyes. Kew Bulletin 1926: 225–238.
- Frederich, M., Tits, M. & Angenot, L., 2008. Potential antimalarial activity of indole alkaloids. Transactions of the Royal Society of Tropical Medicine and Hygiene 102: 11–19.
- Neuwinger, H.D., 2000. African traditional medicine: a dictionary of plant use and applications. Medpharm Scientific, Stuttgart, Germany. 589 pp.
- Oluwafemi, A.J., Okanla, E.O., Camps, P., Munoz-Torrero, D., Mackey, Z.B., Chiang, P.K., Seville, S. & Wright, C.W., 2009. Evaluation of Cryptolepine and Huperzine derivatives as lead compounds towards new agents for the treatment of human African trypanosomiasis. Natural Product Communications 4(2):193–198
- van Miert, S., Hostyn, S., Maes, B. U W, Cimanga, K., Brun, R., Kaiser, M., Matyus, P., Dommisse, R., Lemiere, G., Vlietinck, A. & Pieters, L., 2005. Isoneocryptolepine, a synthetic indoloquinoline alkaloid, as an antiplasmodial lead compound. Journal of Natural Products 68(5): 674–677.
- Wright, C.W., 2007. Recent developments in naturally derived antimalarials: cryptolepine analogues. Journal of Pharmacy and Pharmacology 59(6): 899–904.
Autres références
- Ablordeppey, S.Y., Fan, P., Li, S., Clark, A.M. &. Hufford, C.D., 2002. Substituted indoquinolines as new antifungal agents. Bioorganic & Medicinal Chemistry 10: 1337–1346.
- Adjebeng-Danquah, J., 2003. Viability studies in Cryptolepis sanguinolenta. B.Sc. Agriculture degree thesis, Department of Crop Science, Faculty of Agriculture, Kwame Nkrumah University of Science and Technology, Kumasi, Ghana. 53 pp.
- Amoasi, M.O., 2007. Formulation and in vitro evaluation of crude extract of Cryptolepis sanguinolenta tablets. B.Pharm. Degree Thesis, Faculty of Pharmacy and Pharmaceutical Sciences, College of Health Sciences, Kwame Nkrumah University of Science and Technology, Kumasi, Ghana. 29 pp.
- Ansah, C., Mfoafo, E. A A, Woode, E. & Duwiejua, M., 2008. Anxiogenic effects of an aqueous crude extract of Cryptolepis sanguinolenta (Periplocaceae) in mice. International Journal of Pharmacology 4(1): 20–26.
- Appiah, D.A., 2006. A review on the importance of toxicity testing of herbal medicines and an investigation on the modulation of the sedative effect of diazepam by Cryptolepis. B.Pharm degree thesis, Department of Pharmacognosy, Faculty of Pharmacy and Pharmaceutical Sciences, College of Health Sciences, Kwame Nkrumah University of Science and Technology, Kumasi, Ghana. 33 pp.
- Bierer, D.E., Fort, D.M., Mendez, C.D., Luo-Jian, Imbach, P.A., Dubenko, L.G., Jolad, S.D., Gerber, R.E., Litvak, J., Lu-Qing, Zhang-PingSheng, Reed, M.J., Waldeck, N., Bruening, R.C., Noamesi, B.K., Hector, R.F., Carlson, T.J., King, S.R., Luo, J., Lu, Q. & Zhang, P.S., 1998. Ethnobotanical-directed discovery of the antihyperglycemic properties of cryptolepine: its isolation from Cryptolepis sanguinolenta, synthesis, and in vitro and in vivo activities. Journal of Medicinal Chemistry 41(6): 894–901.
- Ansah, C., Mfoafo, E. A A, Woode, E. & Duwiejua, M., 2008. Anxiogenic effects of an aqueous crude extract of Cryptolepis sanguinolenta (Periplocaceae) in mice. International Journal of Pharmacology 4(1): 20–26.
- Bourdy, G., Willcox, M.L., Ginsburg, H., Rasoanaivo, P., Graz, B. & Deharo, E., 2007. Ethnopharmacology and malaria: New hypothetical leads or old efficient antimalarials? International Journal for Parasitology 38(1): 33–41.
- Bullock, A.A., 1963. Periplocaceae. In: Hepper, F.N. (Editor). Flora of West Tropical Africa. Volume 2. 2nd Edition. Crown Agents for Oversea Governments and Administrations, London, United Kingdom. pp. 80–85.
- Cimanga, K., de Bruyne, T., Pieters, L., Totte, J., Tona, L., Kambu, K., vanden Berghe, D. & Vlietinck, A.J., 1998. Antibacterial and antifungal activities of neocryptolepine, biscryptolepine and cryptoquindoline, alkaloids isolated from Cryptolepis sanguinolenta. Phytomedicine 5(3): 209–214.
- Dassonneville, L., Lansiaux, A., Wattelet, A., Wattez, N., Mahieu, C., Van Miert, S., Pieters L. & Bailly, C., 2000. Cytotoxicity and cell cycle effects of the plant alkaloids cryptolepine and neocryptolepine: Relation to drug-induced apoptosis. European Journal of Pharmacology 409: 9–18.
- Jonckers, T.H., van Miert, S., Cimanga, K., Bailly, C., Colson, P., De Pauw Gillet, M.C., van den Heuvel, H., Claeys, M., Lemiere, F., Esmans, E.L., Rozenski, J., Quirijnen, L., Maes, L., Dommisse, R., Lemiere, G.L., Vlietinck, A. & Pieters, L., 2002. Synthesis, cytotoxicity, and antiplasmodial and antitrypanosomal activity of new neocryptolepine derivatives. Journal of Medicinal Chemistry 45(16): 3497–3508.
- Luo, J., Fort, D.M., Carlson, T.J., Noamesi, B.K., nii-Amon-Kotei, D., King, S.R., Tsai, J., Quan, J., Hobensack, C., Lapresca, P., Waldeck, N., Mendez, C.D., Jolad, S.D., Bierer, D.E. & Reaven, G.M., 1998. Cryptolepis sanguinolenta: an ethnobotanical approach to drug discovery and the isolation of a potentially useful new antihyperglycaemic agent. Diabetic Medicine 15(5): 367–374.
- Mertz, O., Lykke, A.M. & Reenberg, A., 2001. Importance and seasonality of vegetable consumption and marketing in Burkina Faso. Economic Botany 55: 276–289.
- Nettey, N.N., 2003. In vitro conservation of selected medicinal plants using tissue culture techniques. B.Sc. Agriculture degree thesis, Department of Crop Science, Faculty of Agriculture, Kwame Nkrumah University of Science and Technology, Kumasi, Ghana. 41 pp.
- Onyeibor, O., Croft, S.L., Dodson, H.I., Feiz-Hadda, M., Kendrick, H., Millington, N.J., Parapini, S., Phillips, R.M., Seville, S., Shnyder, S.D., Taramelli, D. & Wright, C.W., 2005. Synthesis of some Cryptolepine analogues, assessment of their antimalarial and cytotoxic activities, and consideration of their antimalarial mode of action. Journal of Medicinal Chemistry 48: 2701–2709.
- Paulo, A., Gomes, E.T., Steele, J., Warhurst, D.C. & Houghton, P.J., 2000. Antiplasmodial activity of Cryptolepis sanguinolenta alkaloids from leaves and roots. Planta Medica 66(1): 30–34.
- Paulo, A. & Houghton, P.J., 2003. Chemotaxonomic analysis of the genus Cryptolepis. Biochemical Systematics and Ecology 31: 155–166.
- Silva, O., Duarte, A., Cabrita, J., Pimentel, M., Diniz, A. & Gomes, E., 1996. Antimicrobial activity of Guinea-Bissau traditional remedies. Journal of Ethnopharmacology 50: 55–59.
- Tabuti, J.R.S., Lye, K.A. & Dhillion, S.S., 2003. Traditional herbal drugs of Bulamogi, Uganda: plants, use and administration. Journal of Ethnopharmacology 88: 19–44.
Sources de l'illustration
- Bullock, A.A., 1963. Periplocaceae. In: Hepper, F.N. (Editor). Flora of West Tropical Africa. Volume 2. 2nd Edition. Crown Agents for Oversea Governments and Administrations, London, United Kingdom. pp. 80–85.
Auteur(s)
- P.C.M. Jansen, PROTA Network Office Europe, Wageningen University, P.O. Box 341, 6700 AH Wageningen, Netherlands
- G.H. Schmelzer, PROTA Network Office Europe, Wageningen University, P.O. Box 341, 6700 AH Wageningen, Netherlands
Citation correcte de cet article
Jansen, P.C.M. & Schmelzer, G.H., 2010. Cryptolepis sanguinolenta (Lindl.) Schltr. In: Schmelzer, G.H. & Gurib-Fakim, A. (Editeurs). Prota 11(2): Medicinal plants/Plantes médicinales 2. [CD-Rom]. PROTA, Wageningen, Pays Bas. Consulté le 23 décembre 2024.
- Voir cette page sur la base de données Prota4U.
NB. Cette version révisée a été publiée dans le volume Médicinales - 2. Une version préliminaire est parue dans le volume Colorants et tanins.