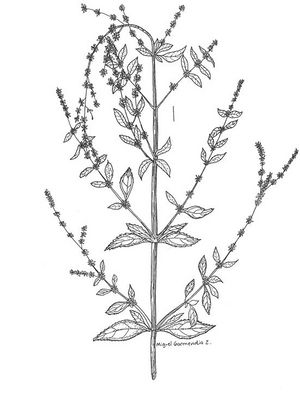
Hyptis verticillata (TRAMIL)
| |
= Hyptis axillaris Fernald = Hyptis parviflora M. Martens & Galeotti
- Nom accepté : Condea verticillata
- Voir sur la TRAMILothèque (davantage d’illustrations)
Sommaire
Noms vernaculaires significatifs TRAMIL
- Nicaragua : trébol de monte, hierba del dolor, escobilla
- Panama : hierba de zorra
- noms créoles : gros baume, gwo bonm, zèb siklon, zèb volkan
Distribution géographique
Herbe amplement distribuée en Amérique tropicale.
Description botanique
Plante herbacée ou suffrutescente pérenne de 1 à 3 m de haut aux rameaux pubérulents. Feuilles menbraneuses, de 3 à 13 cm de long, opposées, lancéolées à ellipticolancéolées, à marge dentellée ou serretée, pubescentes à glabres sur les deux faces, avec des ponctuations résineuses. Inflorescences verticillées à l’aisselle des feuilles supérieures réduites, pédicelles courts ou presque inexistants, formant des pointes interrompues, paniculées, avec 12 à 15 fleurs; calice tubulaire de 2 mm de long; corolle blanche à bleue, un peu pubescente de 2 à 3 mm de long. Fruits, 2 à 4 nucules ovoïdes à oblongues de 1,5 à 1,7 mm de long.
Vouchers :
- Ochoa,243,HPMHV
- FLORPAN,1928,PMA
- Quesada,2842,HCR
Emplois traditionnels significatifs TRAMIL
- maux de tête : feuille, décoction, voie orale1 ; feuille fraîche, nature, application sur le front1
- douleurs d’estomac : racine fraîche, décoction, voie orale2
Recommandations
Selon l’information disponible :
L’emploi contre les maux de tête est classé REC sur la base de l’usage significatif traditionnel documenté dans les enquêtes TRAMIL, les études de toxicité et de validation de l’usage par voie orale.
Si l’état du patient se détériore ou si les maux de tête durent plus de 2 jours, consulter un médecin. L’emploi contre les douleurs d’estomac est classé REC sur la base de l’usage significatif traditionnel documenté dans les enquêtes TRAMIL, les études de toxicité.
Si l’état du patient se détériore ou si les douleurs d’estomac durent plus de 3 jours, consulter un médecin. On ne dispose pas d’information garantissant l’innocuité de son emploi médicinal sur les enfants de moins de 12 ans, ni sur les femmes enceintes ou allaitantes.
Chimie
Les parties aériennes contiennent des lignanes : hiptinine, podophylotoxine, 4’-déméthyl-podophylotoxine3-4, déhydro- méthyl éther de β-peltatine, apo-β-picropodophyline, désoxy-picropodophyline, 5-méthoxy-déhydro-podophylotoxine, 4’déméthyl-désoxy-podophylotoxine, iso-désoxy-podophylotoxine, (-) yatéine5, déhydro-podophylotoxine, désoxy-déhydro-podophylotoxine3-5, podorizol, épi-podorizol3; triterpènes : acides maslinique, oléanolique, ursolique et 2-α-hydroxy-ursolique5, 5(R)-hydroxy-pirrolidine-2-one4, phénylpropanoïdes : acide rosmarinique3-4 et flavonoïde : sidéritoflavone3-5. L’huile essentielle des parties aériennes obtenue par hydro-distillation contient : cadine-4,10(15)-dién-3-one (sesquiterpenoïde) et aromadendr-1(10)-én-9-one (escuamulosone), comme composants majoritaires6. Le bourgeon contient des triterpènes : acide oléanolique, stéroïdes : β-sitostérol7.
La tige et la feuille contiennent des lignanes : β-peltatine, 4’déméthyl-désoxy-podophylotoxine8.
L’huile essentielle de feuille contient des monoterpènes : α et β-pinène, podorizol, epi-podorizol, timol9, cadinadiènone et escuamulosone10; sesquiterpènoïdes : cadine- 4,10(15)-dién-3-one (15,1mL) et aromadendr-1(10)-én-9-one (esquamulosone) (30,7%)10.
Dans la racine, on a isolé les métabolites suivants : 7-acétoxy-16-benzoxy-12-hydroxyabiete-8,12-dién- 11,14-dione, 11,14 dihydroxy-12-méthoxyabiete-8,11,13-trién-7-one, 11,14-dihydroxy-12-méthoxy-18(4-3βH)abeo-abiete-4(19),8,11,13-tetraén-7-one, 7-acétoxy- 12-méthoxyabiete-8,12-dién-11,14-dione, royleanone, 7,6-déhydroroyleanone et 7-acétoxyhorminone11.
Activités biologiques
Travail TRAMIL12
L’extrait aqueux (décoction à 50%) de feuille sèche (1 g/mL), (300, 500, 1000 mg/kg) par voie orale à la souris albinos, modèle anti-inflammatoire par injection de carraghénine, a montré une activité anti-inflammatoire comparable à la déxamétasone.
Travail TRAMIL13
L’extrait aqueux (décoction à 30%) de parties aériennes sèches, (10 μL/chaque face de l’oreille droite), par voie topique à la souris OF-1 (20-25 g), 6 mâles/groupe, modèle d’inflammation induite par l’huile de Croton (1% en acétone). L’oreille gauche a reçu de l’acétone (10 μL). On a observé une réduction légère (15%) statistiquement significative de l’inflammation.
Travail TRAMIL14
L’extrait aqueux (décoction à 30%) de parties aériennes sèches (0,5, 1, 5 et 10 g de matériel végétal/kg) par voie orale à la souris OF-1 mâle (20-25 g), 10 animaux/groupe, modèles de contorsions induite par l’acide acétique (0,75%) intrapéritonéal (0,1 mL/10 g) et du retrait de la queue provoqué par immersion dans l’eau chaude (55°C). Seule la dose de 10 g/kg modèle de contorsions a montré une activité analgésique significative, les autres doses et modèles restant sans réponse.
Travaux TRAMIL15-16
L’extrait aqueux (décoction) de racine fraîche, en dose unique de 1 mL/animal (4,0 mg ± 0,2 mg de solides totaux/mL) par voie orale à la souris Swiss (CD-1), (15 mâles de 22,06 ± 1,68 g et 10 femelles de 17,10 ± 0,53 g), et dans un autre essai avec administration quotidienne durant 6 jours consécutifs à 5 souris femelles (21,60 ± 0,40 g) et 5 mâles (25,20 ± 0,73 g), à jeun depuis 6 heures, les groupes témoin ayant reçu 1 mL d’eau distillée par animal, le charbon actif étant utilisé comme marqueur. On a pas observé de modification de la vitesse de transit intestinal.
Toxicité
Travail TRAMIL17
L’extrait aqueux (décoction) de feuille fraîche et bourgeon frais, lyophilisés, (1 g/kg), 5 jours consécutifs par semaine, durant 55 jours, par voie orale à la souris NGP (5 mâles et 5 femelles), n’a pas provoqué de mort, ni d’autres signes évidents de toxicité pendant les 14 jours d’observation postérieurs au traitement.
Travail TRAMIL12
L’extrait aqueux (décoction) 0,5 g/mL de feuille sèche (4 g/kg = 8 mL/kg) par voie topique sur peau saine du dos de 9 lapins albinos New Zealand souche UniValle, modèle de Draize modifié par Finkelstein, n’a provoqué aucune altération locale d’irritabilité topique.
Travail TRAMIL18
L’extrait aqueux (décoction) de racine fraîche, 1 mL/ animal/5 jours (4 mg ± 0,2 mg de solides totaux/mL), par voie orale à la souris Swiss (CD-1) (5 mâles et 5 femelles de 23,1 ± 0,83 g). Le témoin a été réalisé avec de l’eau distillée sur 10 autres souris de mêmes caractéristiques. Pendant l’essai ni pendant la période d’observation postérieure de 10 jours, ne s’est présenté de mortalité, ni de signe évident de toxicité . L’étude macroscopique des organes internes n’a montré aucune lésion.
On ne dispose pas d’information sur l’innocuité de son emploi avec des enfants, ou des femmes enceintes ou allaitantes.
Préparation et dosage
Contre les maux de tête :
Préparer une décoction avec 7-8 feuilles fraîches (2 grammes) dans 2 tasses (500 millilitres) d’eau, faire bouillir pendant 10 minutes dans un récipient ouvert. Laisser refroidir, filtrer et boire 1 tasse, 2 fois par jour pendant un maximum de 2 jours1.
Contre les douleurs d’estomac :
Préparer une décoction avec 15 grammes de racine dans 4 tasses (1 litre) d’eau; faire bouillir pendant 10 minutes dans un récipient couvert. Laisser refroidir, filtrer et boire 1 tasse 15 minutes avant chaque repas.
Toute préparation médicinale doit être conservée au froid et utilisée dans les 24 heures.
Références
- SOLIS PN, CORREA M, GUPTA MP, 1995 Encuesta TRAMIL (Comunidades afro-caribeñas). Centro de Investigaciones Farmacognósticas de la Flora Panameña CIFLORPAN, Facultad de Farmacia, Universidad de Panamá, Panamá, Panamá.
- AKER CH, GARMENDIA M, DEVES R, FERNANDEZ P, FRITHZ E, HERNANDEZ M, SIMEON A, 2003 Encuesta TRAMIL (Bosawas). Departamento de Biologia, Facultad de Ciencias, Universidad Nacional Autónoma de Nicaragua UNAN-León, León, Nicaragua.
- KUHNT M, RIMPLER H, HEINRICH M, 1994 Lignans and other compounds from the mixe Indian medicinal plant Hyptis verticillata. Phytochemistry 36(2):485-489.
- KUHNT M, PROBSTLE A, RIMPLER H, BAUER R, HEINRICH M, 1995 Biological and pharmacological activities and further constituents of Hyptis verticillata. Planta Med 61(3):227-232.
- NOVELO M, CRUZ JG, HERNANDEZ L, PEREDA R, CHAI H, MAR W, PEZZUTO JM, 1993 Cytotoxic constituents from Hyptis verticillata. J Nat Prod 56(10):1728- 1736.
- FACEY PC, PORTER RB, REESE PB, WILLIAMS LA, 2005 Biological activity and chemical composition of the essential oil from Jamaican Hyptis verticillata Jacq. J Agric Food Chem 53(12):4774-4777.
- DOMINGUEZ XA, ALCORN JB, 1985 Screening of medicinal plants used by Huastec Mayans of Northeastern Mexico. J Ethnopharmacol 13(2):139-156.
- GERMAN VF, 1971 Isolation and characterization of cytotoxic principles from Hyptis verticillata. J Pharm Sci 60(4):649-650.
- DUKE J, 1992 Handbook of biologically active phytochemicals and their activities. Boca Ratón, USA: CRS Press, 183pp.
- FACEY PC, PORTER RB, REESE PB, WILLIAMS LA, 2005 Biological activity and chemical composition of the essential oil from Jamaican Hyptis verticillata Jacq. J Agric Food Chem 53(12):4774-4777.
- PORTER RB, BIGGS DA, REYNOLDS WF, 2009 Abietane diterpeniods from Hyptis verticillata. Nat Prod Commun 4(1):15-18.
- HERRERA J, 1992 Determinación de parámetros farmacológicos usados en medicina tradicional popular en la Cuenca del Caribe. Informe TRAMIL. Dep. de Farmacología, Facultad de Salud, Universidad del Valle, Cali, Colombia.
- FRIAS I, CABRERA H, GARCIA N, MORON FJ, VICTORIA MdC, MOREJON Z, NOSSIN E, 2011 Efecto antiinflamatorio tópico de la decocción de partes aéreas secas de Hyptis verticillata en ratones. Informe TRAMIL. Facultad de Ciencias Médicas “Dr. Salvador Allende”, Laboratorio Central de Farmacología, La Habana, Cuba.
- MORON FJ, LOPEZ M, VICTORIA MdC, MOREJON Z, NOSSIN E, BOUCOURT E, FUENTES V, 2008 Acción analgésica de la decocción de partes aéreas secas de Hyptis veticillata Jacq. en ratones. Informe TRAMIL. Facultad de Ciencias Médicas “Dr. Salvador Allende”, Laboratorio Central de Farmacología, La Habana, Cuba.
- GARCIA M, LIZANO V, BERROCAL B, ZUNIGA I, 2009 Velocidad del tránsito intestinal en ratones del extracto acuoso de la raíz fresca de Hyptis verticillata, dosis única. Informe TRAMIL. PRONAPLAMED. Depto. de Fisiología, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
- GARCÍA M, BERROCAL B, MONERA L, SOLE M, ZUNIGA I, 2010 Velocidad del tránsito intestinal en ratones, del extracto acuoso de la raíz fresca de Hyptis verticillata, dosis repetida. Informe TRAMIL. PRONAPLAMED. Depto. de Fisiología, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
- GARCIA M, COTO MT, GONZALEZ CS, PAZOS L, 1996 Toxicidad sub-crónica en ratones, del extracto acuoso de hojas y cogollos frescos de Hyptis verticillata. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
- GARCIA M, LIZANO V, BERROCAL B, ZUNIGA I, 2009 Toxicidad aguda dosis repetida, en ratones, del extracto acuoso de raíz fresca de Hyptis verticillata. Informe TRAMIL. PRONAPLAMED. Depto de Fisiología, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.