Milicia excelsa (PROTA)
Introduction |
| Importance générale | |
| Répartition en Afrique | |
| Répartition mondiale | |
| Fruit | |
| Légume | |
| Colorant / tanin | |
| Médicinal | |
| Bois d'œuvre | |
| Bois de feu | |
| Ornemental | |
| Fibre | |
| Sécurité alimentaire | |
| Statut de conservation | |
Milicia excelsa (Welw.) C.C.Berg
- Protologue: Bull. Jard. Bot. Belg. 52: 227 (1982).
- Famille: Moraceae
Synonymes
- Maclura excelsa (Welw.) Bureau (1873),
- Chlorophora excelsa (Welw.) Benth. (1880).
Noms vernaculaires
- Iroko, chêne d’Afrique, teck d’Afrique, teck kambala (Fr).
- Iroko, rock elm, African teak, African oak (En).
- Câmbala, amoreira, moreira, teca africana, tumbiro, magundo (Po).
- Mvule (Sw).
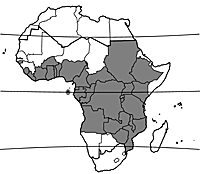
Origine et répartition géographique
L’aire de répartition de Milicia excelsa s’étend depuis la Guinée-Bissau jusqu’à l’Ethiopie, et vers le sud jusqu’à l’Angola, au Zimbabwe et au Mozambique. Il a été introduit en Inde et aux Etats-Unis.
Usages
Le bois de Milicia excelsa et celui de l’espèce très voisine Milicia regia (A.Chev.) C.C.Berg ne sont pas distingués dans le commerce des bois, et sont commercialisés sous le même nom commercial d’ “iroko”, ou “odum” au Ghana. D’autres noms commerciaux fréquemment employés pour Milicia excelsa sont “kambala” et “mvule”. L’iroko est une essence commerciale très appréciée en Afrique, pour laquelle la demande est importante. Il est employé comme bois de construction, pour la construction navale et la charpenterie de marine, les traverses de chemin de fer, les portes d’écluse, les charpentes, les chariots, les égouttoirs, les menuiseries extérieures et intérieures, les escaliers, les portes, les encadrements, les meubles de jardin, l’ébénisterie, les panneautages, la parqueterie, les planches profilées pour la décoration et la charpente. On l’emploie aussi pour les objets sculptés, les ustensiles domestiques, les instruments de musique et les jouets. Comme il est résistant aux acides et aux bases, on l’emploie pour faire des cuves et des barils pour les aliments et les produits chimiques, ainsi que des paillasses de laboratoire. On l’emploie en placages tranchés mais rarement en placages déroulés. Le bois est également utilisé en bois de feu et pour faire du charbon de bois.
Les fruits mûrs et les jeunes feuilles bouillies de Milicia excelsa sont comestibles. Le jus du fruit est employé en Inde comme condiment. Les feuilles mûres ont été employées en guise de papier de verre. L’écorce est employée pour teindre les cuirs et les tissus, et pour couvrir les maisons. Autrefois, l’écorce des jeunes arbres était utilisée pour faire des pagnes. L’arbre est employé pour la conservation des sols et la production de paillis, et comme arbre d’ornement et d’ombrage. Au Nigeria, on le plante pour marquer les limites entre exploitations agricoles ou entre villages. On l’a aussi planté pour attirer des chenilles comestibles. Le bois est à l’essai comme substrat pour la culture du champignon Lentinus subnudus, apprécié par ex. au Nigeria.
Milicia excelsa est largement utilisé en médecine africaine traditionnelle. Une décoction de racines sert à traiter la stérilité féminine. Une décoction d’écorce des racines et du tronc est absorbée comme aphrodisiaque. Des préparations à base d’écorce sont administrées pour traiter la toux, l’asthme, les affections cardiaques, le lumbago, les douleurs de la rate, les maux d’estomac, les douleurs abdominales, l’œdème, l’ascite, la dysménorrhée, la blennorragie, la fatigue générale, les rhumatismes, les entorses, ainsi que comme galactagogue, aphrodisiaque, tonique et purgatif. Des préparations à base d’écorce sont appliquées par voie externe pour traiter la gale, les blessures, la chute des cheveux, la fièvre, les maladies vénériennes et les entorses. On les administre en lavement pour soigner les hémorroïdes, la diarrhée et la dysenterie. Le latex est appliqué sur les brûlures, les blessures, les plaies, ainsi que contre l’eczéma et autres affections de la peau. On l’absorbe également contre les problèmes d’estomac, l’hypertension et comme galactogène, et on l’emploie pour le traitement des tumeurs et les obstructions de la gorge. Les feuilles sont mangées pour traiter la folie ; une macération de feuilles est absorbée comme galactagogue. On boit une décoction de feuilles pour traiter les calculs biliaires. Des préparations de feuilles en application externe servent à traiter les morsures de serpents et la fièvre, et en gouttes oculaires elles servent à traiter la filariose.
Milicia excelsa et souvent considéré comme un arbre sacré, et il est fréquemment protégé près des habitations et dans les champs cultivés. Au Bénin, le feuillage est employé comme fétiche, et au Nigeria l’arbre a une place spéciale dans le folklore et les traditions populaires.
Production et commerce international
Milicia excelsa et Milicia regia sont tous deux commercialisés sous le nom d’iroko, et la part de Milicia excelsa dans ce commerce est inconnue. L’iroko est un bois d’œuvre important dans le commerce international ; au cours des années 1960, la Côte d’Ivoire a exporté environ 55 000 m³ d’iroko en grumes et 6000 m³ de sciages d’iroko par an, et le Ghana 28 000 m³ de sciages. En 1973, la Côte d’Ivoire a exporté un maximum de 136 500 m³ d’iroko en grumes et 16 000 m³ de sciages. En 1994, le Cameroun a exporté 65 000 m³ de grumes et 12 000 m³ de sciages, le Congo 10 000 m³ de grumes, et le Ghana au moins 47 000 m³ de sciages. Au cours de la saison 1998–99, on a estimé à 133 400 m³ le volume de bois d’iroko abattu au Cameroun. De 1998 à 2003, le Gabon a exporté environ 28 500 m³ de grumes par an. L’exportation d’iroko en grumes est désormais interdite en Côte d’Ivoire, au Ghana et au Cameroun, mais l’exportation en sciages est autorisée.
En 2003, le Cameroun a exporté 33 000 m³ de sciages d’iroko (US$ 948/m³), le Congo 28 000 m³ d’iroko en grumes (US$ 221/m³) et 1000 m³ de placages d’iroko (US$ 343/m³), la Centrafrique 2000 m³ de grumes (US$ 412/m³) et 5000 m³ de sciages (US$ 465/m³), le Ghana 8000 m³ de sciages (US$ 754/m³), et le Togo 1000 m³ de sciages (US$ 260/m³).
Dans le passé, la Tanzanie et l’Ouganda étaient d’importants fournisseurs d’iroko, et il en est encore exporté de faibles volumes d’Afrique de l’Est.
Propriétés
Le bois de cœur est jaune pâle à jaune, virant lorsqu’il est exposé au brun jaunâtre ou brun verdâtre, ou parfois au brun chocolat ; il est nettement distinct de l’aubier blanc jaunâtre, épais de 5–7,5 cm. Il est contrefil, le grain est moyen à grossier, avec une figure moirée. Le bois est un peu gras et inodore. Les grumes provenant de forêt fermée sont en général rectilignes et cylindriques, tandis que les arbres de savane sont souvent endommagés par le feu, et leur bois est atteint de croissance excentrée, d’entre-écorce ou d’inclusions de carbonate de calcium.
Le bois a une densité de 550–750 kg/m³ à 12% d’humidité. Les taux de retrait de l’état vert à anhydre sont de 1,7–4,1(–5,6)% dans le sens radial et 2,4–6,3(–9,8)% dans le sens tangentiel. Le bois se sèche bien à l’air et en séchoir, avec peu de dégradation. Des planches épaisses de 4,2 cm peuvent être séchées en séchoir de 60% à 15% d’humidité en 8 jours à une température de séchage de 50–80°C, et une humidité relative correspondante de 85% à 40%. Une fois que le bois est sec, il bouge peu en service.
A 12% d’humidité, le module de rupture est de 75–156 N/mm², le module d’élasticité de 8300–13 300 N/mm², la compression axiale de 42–65 N/mm², le cisaillement de 5,4–14,1 N/mm², le fendage de 10,3–20,9 N/mm, la dureté de flanc Janka de 4400–5610 N, et la dureté en bout Janka de 5360–6640 N.
Les caractéristiques de travail aux outils à main et mécaniques sont généralement bonnes mais variables ; le contrefil peut gêner le sciage et le rabotage. Le bois est assez abrasif en raison de la présence de dépôts durs (“pierres d’iroko”, formés principalement de carbonate de calcium), qui peuvent émousser les tranchants d’outils. La déchirure lors du rabotage peut être évitée en employant des angles de coupe de 15° ou moins. Le bois a de bonnes caractéristiques de clouage, vissage, mortaisage et collage, et se tourne aisément. Il se finit bien, mais un enduit bouche-pores est nécessaire. Le bois contient un dérivé du stilbène, la chlorophorine, qui empêche les peintures à base d’huile de sécher, et qui corrode les métaux avec lesquels il est en contact. Les caractéristiques de cintrage à la vapeur du bois sont moyennes.
Bien que le bois de cœur soit généralement considéré comme très durable, les données rapportées sur sa résistance aux térébrants marins et aux termites sont variables. Il est résistant aux attaques de champignons. L’aubier est sujet aux attaques de Lyctus. Le bois de cœur est imperméable aux produits d’imprégnation, mais l’aubier leur est perméable.
Le bois et la sciure peuvent provoquer des dermatites, une irritation des voies nasales et de la gorge, et des réactions asthmatiques, dues à la présence de chlorophorine. Ce composé a montré des effets inhibiteurs sur la biosynthèse de la mélanine ; son dérivé plus stable, l’hexahydrochlorophorine, peut avoir des usages potentiels dans des agents de blanchiment de la peau et pour traiter les troubles de la pigmentation. Deux composés phénoliques (chlorophorine et iroko) ont montré in vitro une action anti-amibienne. Un extrait au méthanol de l’écorce du tronc a montré in vivo des propriétés anti-inflammatoires chez les souris et les rats.
Falsifications et succédanés
Les caractéristiques du bois d’iroko sont comparables à celles du teck (Tectona grandis L.f.). Le bois de Guibourtia arnoldiana (De Wild. & T.Durand) J.Léonard (nom commercial : mutenye) est employé aux mêmes usages que l’iroko et le teck. Comme l’iroko est localement surexploité, il est recommandé de lui substituer pour certains usages spécifiques des essences telles que Piptadeniastrum africanum (Hook.f.) Brenan (nom commercial : dabéma), Lophira alata Banks ex P.Gaertn. (nom commercial : azobé), Nauclea diderrichii (De Wild. & T.Durand) Merr. (nom commercial : bilinga) ou Afzelia spp. (nom commercial : doussié). Des grumes de Morus mesozygia Stapf ex A.Chev. (nom commercial : difou) sont parfois vendues en mélange avec des grumes d’iroko.
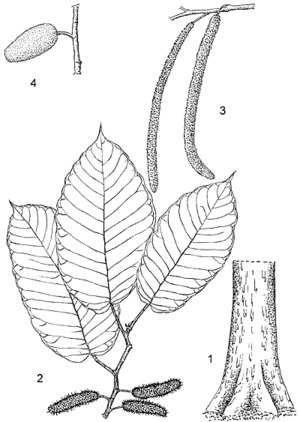
Description
- Grand arbre dioïque atteignant 50 m de haut ; fût rectiligne, cylindrique, dépourvu de branches sur une longueur atteignant 25(–30) m, jusqu’à 2,5(–3) m de diamètre, contreforts absents ou peu développés ; racines superficielles souvent longues et proéminentes, brun-rouge avec des lenticelles jaunes ; écorce externe grise à brun foncé ou noire, à lenticelles, devenant écailleuse, écorce interne épaisse, fibreuse, de couleur crème avec des mouchetures brun-rouge, exsudant un latex blanc ou jaunâtre ; cime étalée ; branches obliquement ascendantes.
- Feuilles alternes distiques, simples ; stipules libres, embrassant légèrement la tige, jusqu’à 5 cm de long, caduques ; pétiole de 1–6 cm de long ; limbe oblong à elliptique, de 6–20 (–33) cm × 3,5–10(–15) cm, base cordée à obtuse, souvent très inégale, apex acuminé, bord presque entier à ondulé mais denté sur les spécimens juvéniles, papyracé à coriace, presque glabre ou légèrement poilu en dessus sur les nervures principales, dessous à pubescence dense et courte entre les nervures les plus fines, pennatinervé à 10–22 paires de nervures latérales.
- Inflorescence : chaton, généralement solitaire à l’aisselle des feuilles ou sur des nœuds non feuillés à la base des rameaux, à pubescence blanche, fleurs nombreuses sur des rangs longitudinaux alternant avec des rangs de bractées ; inflorescence mâle de 8–20(–32) cm × 0,5–1 cm, pendante, pédoncule de 0,5–2,5 cm de long ; inflorescence femelle de 2–4 cm × 0,5–2 cm, pédoncule de 0,5–2 cm de long.
- Fleurs unisexuées, 4-mères, sessiles ; fleurs mâles d’environ 1,5 mm de long, blanches, tépales 4, soudés à la base, étamines 4, courbées dans le bouton, pistil rudimentaire présent ; fleurs femelles de 2–3 mm de long, à 4 tépales soudés à la base, verdâtres, ovaire supère, d’environ 1 mm de long, 1-loculaire, stigmates 2, l’un de 3–7 mm de long, l’autre jusqu’à 1 mm de long.
- Fruit : akènes ellipsoïdes, comprimés, de 2,5–3 mm de long, disposés en infrutescence jusqu’à 5 cm × 1,5 cm.
- Graines d’environ 2 mm de long.
- Plantule à germination épigée.
Autres données botaniques
Le genre Milicia comprend 2 espèces, Milicia regia et Milicia excelsa, poussant toutes deux en Afrique tropicale. Les 2 espèces diffèrent principalement par la nervation et la pubescence des feuilles. Milicia excelsa a 10–22 paires de nervures latérales, avec une courte pubescence sur la face inférieure entre les nervures les plus fines, tandis que Milicia regia a 6–11 paires de nervures latérales et est glabre sur la face inférieure entre les nervures les plus fines. Les individus juvéniles des deux espèces peuvent être distingués par des différences dans la pubescence des feuilles et dans la couleur de la nervure médiane sur la face inférieure (jaune chez Milicia excelsa, rouge chez Milicia regia), ainsi que dans le mode de croissance et la disposition des feuilles (mode sympodial et feuilles disposées en deux rangées chez Milicia excelsa; mode monopodial et feuilles disposées en spirale chez Milicia regia).
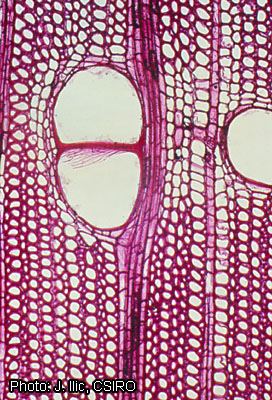
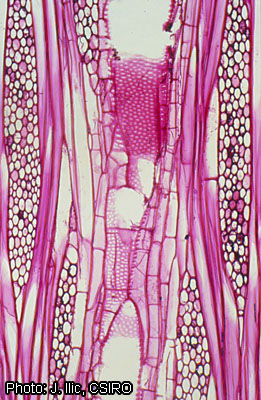
Anatomie
Description anatomique du bois (codes IAWA pour les bois feuillus) :
- Cernes de croissance : 2 : limites de cernes indistinctes ou absentes.
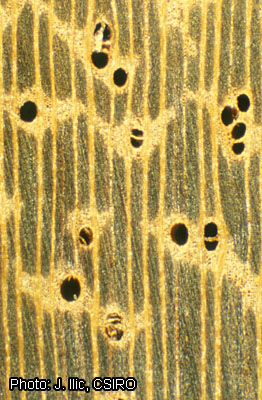
- Vaisseaux : 5 : bois à pores disséminés ; 13 : perforations simples ; 22 : ponctuations intervasculaires en quinconce ; 23 : ponctuations alternes (en quinconce) de forme polygonale ; 27 : ponctuations intervasculaires grandes (≥ 10 μm) ; (30 : ponctuations radiovasculaires avec des aréoles distinctes ; semblables aux ponctuations intervasculaires en forme et en taille dans toute la cellule du rayon) ; 31 : ponctuations radiovasculaires avec des aréoles très réduites à apparemment simples : ponctuations rondes ou anguleuses ; 32 : ponctuations radiovasculaires avec des aréoles très réduites à apparemment simples : ponctuations horizontales (scalariformes) à verticales (en balafres) ; 43 : diamètre tangentiel moyen du lumen des vaisseaux ≥ 200 μm ; 46 : ≤ 5 vaisseaux par millimètre carré ; (47 : 5–20 vaisseaux par millimètre carré) ; 56 : thylles fréquents.
- Trachéides et fibres : 61 : fibres avec des ponctuations simples ou finement (étroitement) aréolées ; 66 : présence de fibres non cloisonnées ; 69 : fibres à parois fines à épaisses.
- Parenchyme axial : 80 : parenchyme axial circumvasculaire étiré ; (81 : parenchyme axial en losange) ; (82 : parenchyme axial aliforme) ; 83 : parenchyme axial anastomosé ; (84 : parenchyme axial paratrachéal unilatéral) ; (85 : parenchyme axial en bandes larges de plus de trois cellules) ; (86 : parenchyme axial en lignes minces, au maximum larges de trois cellules) ; 91 : deux cellules par file verticale ; 92 : quatre (3–4) cellules par file verticale.
- Rayons : 98 : rayons couramment 4–10-sériés ; 106 : rayons composés de cellules couchées avec une rangée terminale de cellules dressées et/ou carrées ; (107 : rayons composés de cellules couchées avec 2 à 4 rangées terminales de cellules dressées et/ou carrées) ; 115 : 4–12 rayons par mm.
- Eléments sécrétoires et variantes cambiales : 132 : laticifères ou tubes à tanins.
- Inclusions minérales : 136 : présence de cristaux prismatiques ; 137 : cristaux prismatiques dans les cellules dressées et/ou carrées des rayons ; 141 : cristaux prismatiques dans les cellules non cloisonnées du parenchyme axial ; (154 : plus d’un cristal approximativement de même taille par cellule ou par loge (dans les cellules cloisonnées)) ; (155 : cristaux de deux tailles différentes par cellule ou par loge).
Croissance et développement
Les graines germent normalement dans les 2–4 semaines suivant le semis. Les jeunes arbres de Milicia excelsa ont une croissance continue, tandis que la croissance des arbres adultes est périodique. A la saison sèche, Milicia excelsa perd ses feuilles pendant une courte période. De l’Afrique de l’Ouest jusqu’au Soudan, il fleurit de décembre à mars. Il s’écoule 5–6 semaines depuis la fertilisation jusqu’à la maturation des fruits. Les graines sont dispersées principalement par les oiseaux, les chauves-souris et les écureuils.
Dans une plantation âgée de 6 ans dans le nord de la Côte d’Ivoire, certains sujets avaient plus de 6 m de hauteur, mais il y avait une large variabilité. Au Ghana, l’accroissement annuel en diamètre est de 0,33–0,59 cm. Au Cameroun, on a enregistré un accroissement moyen en diamètre de plus de 1 cm par an sur des arbres âgés d’environ 25 ans. Dans le sud-ouest de la Centrafrique (pluviométrie annuelle 1500 mm ; période sèche de 2 mois), l’accroissement annuel moyen en diamètre de sujets de Milicia excelsa est de 0,57 cm ; il décroît avec l’âge : de 0,93 cm pour des arbres d’un diamètre inférieur à 10 cm à 0,45 cm pour des arbres de 110–120 cm de diamètre. Dans cette région il faut en moyenne 130 ans à un arbre pour atteindre un diamètre de 80 cm. En Ouganda, des arbres de 32 ans plantés à un espacement de 4 m × 4 m avaient 18 m de hauteur, avec une bonne forme.
Ecologie
Milicia excelsa se rencontre dans la forêt décidue, semi-décidue ou sempervirente, primaire ou secondaire, avec une préférence manifeste pour les types de forêt les plus secs. On le trouve souvent dans des forêts-galerie et des îlots de forêt ou à l’état isolé dans les régions de savane, et il subsiste parfois à l’état isolé dans les anciennes zones cultivées. On le trouve généralement jusqu’à 1200(–1500) m d’altitude, mais on l’a trouvé jusqu’à 4500 m d’altitude sur le mont Kilimandjaro en Tanzanie. En Afrique de l’Ouest, Milicia excelsa pousse dans des régions ayant une température moyenne annuelle de 25–35°C et une pluviométrie annuelle moyenne de 1150–1900 mm. Il est considéré comme une essence pionnière exigeant une lumière intense et incapable de supporter une ombre épaisse. Dans une jeune forêt secondaire, par exemple, il ne supporte pas la concurrence des lianes et des arbustes.
Bien que Milicia excelsa pousse sur une large variété de sols, il est réputé plutôt exigeant quant à la fertilité du sol, surtout en ce qui concerne la présence de K et de P. Il est considéré comme un indicateur de sol fertile convenant à la culture. Il préfère des sols bien drainés, et ne tolère pas les sols engorgés.
Multiplication et plantation
Milicia excelsa est multiplié principalement par graines. Le poids de 1000 graines est de 1–4 g. Il faut environ 40 kg de fruits pour obtenir 1 kg de graines. Etant donné que la couleur des infrutescences ne change pas au cours du mûrissement, la maturité doit être déterminée en coupant l’infrutescence pour voir si la pulpe s’est ramollie. Si l’on a récolté sur l’arbre des infrutescences non mûres, il faut les laisser à l’ombre pendant quelques jours pour qu’elles mûrissent. Il est plus facile de les récolter sur le sol, mais les graines doivent être extraites avant que les infrutescences commencent à fermenter. On peut séparer les graines en écrasant les infrutescences après les avoir immergées dans l’eau pendant une journée environ. Les graines viables coulent dans l’eau et peuvent être aisément séparées des graines vaines qui flottent. Les graines fraîches germent normalement bien ; le taux de germination peut être de plus de 90% en 4 semaines. Il vaut mieux semer dans les 3 mois suivant la récolte, car la viabilité des graines décroît rapidement. Des graines séchées jusqu’à 8% de teneur en humidité peuvent être entreposées pendant au moins un an à 0–5°C.
Les graines sont semées sur une planche de semis, et les semis sont repiqués dans des pots ou sur des planches de pépinière 3 semaines après la germination. Il faut les maintenir sous ombrage afin de limiter les attaques de Phytolyma spp. Environ 4 mois après le semis les jeunes plants ont environ 30 cm de haut, et sont prêts à replanter sur le terrain. Les jeunes plants supportent bien la transplantation. Au Ghana, des jeunes plants transplantés durant la longue saison des pluies ont montré une bien meilleure croissance que ceux transplantés durant la petite saison des pluies. Cette croissance meilleure a persisté pendant au moins 9 ans. Une plantation en peuplement mixte avec Terminalia superba Engl. & Diels (en proportions égales à la mise en place) a fourni une meilleure croissance qu’une plantation en peuplements purs.
Milicia excelsa peut être multiplié végétativement par boutures de tige et de racine, greffage, marcottage et culture de tissus in vitro. On a obtenu une multiplication réussie en employant des boutures provenant d’arbres de 1 et 2 ans, tandis qu’avec des arbres adultes les boutures doivent être prélevées sur des rejets de souche. Des pieux et des poteaux tirés de branches peuvent prendre racine comme des boutures.
Du fait de la grande largeur de l’aubier de Milicia excelsa, les produits d’éclaircie des plantations ont peu de valeur, c’est pourquoi il est recommandé de planter à larges écartements.
Gestion
Milicia excelsa est principalement extrait de la forêt naturelle, du fait que les plantations souffrent fortement des attaques d’insectes. Il s’élague bien, et rejette bien de souche.
Maladies et ravageurs
La principale contrainte pour les plantations de Milicia excelsa et Milicia regia est constituée par les attaques d’insectes responsables de galles (Phytolyma spp.). Ceux-ci déposent leurs œufs sur des bourgeons, sur de jeunes pousses ou sur de jeunes feuilles, et après la sortie des nymphes il se forme des galles, suivies par le dépérissement du feuillage jusqu’au tissu ligneux. Cela interrompt les processus physiologiques, provoque une réduction de la croissance, et dans de nombreux cas tue les semis. Une infection secondaire par des champignons aggrave probablement les dégâts. Les feuilles adultes ne sont pas sérieusement touchées. Les efforts pour lutter contre ce parasite n’ont guère eu de succès, mais la création ou la sélection de génotypes de Milicia plus résistants pourrait offrir des perspectives. La plantation dans une ombre légère, en mélange et à faible densité semble aider à réduire les dégâts de Phytolyma. Les éléphants mangent l’écorce et peuvent détruire les plantations.
Rendement
Au Gabon, Milicia excelsa se rencontre disséminé dans tous les types de forêts, avec un volume commercial de fût de l’ordre de 0,1 m³/ha.
Traitement après récolte
Immédiatement après l’abattage, le bois de Milicia excelsa est trop lourd pour pouvoir être transporté par flottage sur les cours d’eau, et le transport se fait par camions. L’aubier est généralement éliminé avant l’expédition par bateau. L’écorce destinée à des usages médicinaux est parfois pilée, séchée et comprimée pour être mise en balles, qui sont préservées emballées.
Ressources génétiques
L’exploitation se fait souvent sans souci de régénération : dans les années 1980, le rythme d’extraction de bois d’iroko (provenant de Milicia excelsa et Milicia regia) au Ghana était estimée à environ 173 000 m³ par an, alors que la régénération des peuplements était estimée à seulement 29 000 m³ par an. Milicia excelsa est classé dans la Liste rouge des espèces menacées 2006 de l’UICN comme espèce “à faible risque mais quasi-menacée”, les principales menaces étant la perte et la dégradation de son milieu du fait de l’expansion de l’agriculture, de la surexploitation de son bois et des attaques de Phytolyma. Milicia excelsa est considéré comme prioritaire pour la conservation in situ. Etant donné que la diversité génétique intra-population est faible, mais que la diversité inter-population est forte, il est recommandé d’inclure différentes populations dans les programmes de conservation in situ. Cela peut être facilité par le fait que dans certaines zones Milicia excelsa est conservé sur les exploitations agricoles, dans des bois sacrés, dans des lieux publics et dans des cimetières. Il est protégé par la loi en Côte d’Ivoire et au Mozambique ; au Ghana et en Tanzanie, un permis est exigé pour son exploitation. Il fait l’objet d’une interdiction d’exportation en grumes dans divers pays, tels que la Côte d’Ivoire, le Ghana, le Cameroun et la Tanzanie.
Sélection
On a reconnu une résistance génétique partielle aux Phytolyma dans des populations naturelles de Milicia, ce qui pourrait conduire à la création de lignées résistantes pour une multiplication végétative. Un travail de sélection est en cours au Ghana.
Perspectives
L’iroko fait partie des bois les plus précieux en Afrique, en raison de son bel aspect, de sa durabilité, de sa stabilité et de ses bonnes caractéristiques d’usinage. A présent son exploitation dans la plupart des pays n’est pas durable. Il nécessite une protection, et son exploitation doit être limitée si l’on veut ménager l’avenir. La plantation est difficile en raison des problèmes de parasites. La recherche de sources de résistance aux galles de l’iroko mérite une haute priorité, et pourrait éventuellement être complétée par le développement de méthodes de lutte efficaces, notamment l’emploi de parasites ou prédateurs naturels de Phytolyma.
Références principales
- Berg, C.C., 1977. Revisions of African Moraceae (excluding Dorstenia, Ficus, Musanga and Myrianthus). Bulletin du Jardin Botanique National de Belgique 47(3–4): 267–407.
- Berg, C.C., 1982. The reinstatement of the genus Milicia Sim (Moraceae). Bulletin du Jardin Botanique National de Belgique 52(1–2): 225–229.
- Berg, C.C. & Hijman, M.E.E., 1989. Moraceae. In: Polhill, R.M. (Editor). Flora of Tropical East Africa. A.A. Balkema, Rotterdam, Netherlands. 95 pp.
- Bolza, E. & Keating, W.G., 1972. African timbers: the properties, uses and characteristics of 700 species. Division of Building Research, CSIRO, Melbourne, Australia. 710 pp.
- Burkill, H.M., 1997. The useful plants of West Tropical Africa. 2nd Edition. Volume 4, Families M–R. Royal Botanic Gardens, Kew, Richmond, United Kingdom. 969 pp.
- Cobbinah, J.R. & Wagner, M.R., 1995. Phenotypic variation in Milicia excelsa to attack by Phytolyma lata (Psyllidae). Forest Ecology and Management 75(1–3): 147–153.
- Ofori, D.A., 2001. Genetic diversity and its implications for the management and conservation of Milicia species. PhD thesis, University of Aberdeen, United Kingdom. 158 pp.
- Ofori, D.A., Swaine, M.D., Leifert, C., Cobbinah, J.R. & Price, A.H., 2001. Population genetic structure of Milicia species characterised by using RAPD and nucleotide sequencing. Genetic Resources and Crop Evolution 48: 637–647.
- Takahashi, A., 1978. Compilation of data on the mechanical properties of foreign woods (part 3) Africa. Shimane University, Matsue, Japan, 248 pp.
- UNEP-WCMC, 2006. Contribution to an evaluation of tree species using the new CITES Listing Criteria. UNEP World Conservation Monitoring Centre, Cambridge, United Kingdom. [Internet]. http://www.unep-wcmc.org/species/tree_study/contents1_en.htm. October 2006.
Autres références
- Apetorgbor, M., Mancini, F., Turco, E., Cobbinah, J.R. & Ragazzi, A., 2001. The involvement of fungal pathogens in dieback-decline of Milicia excelsa saplings in plantations. Zeitschrift fuer Pflanzenkrankheiten und Pflanzenschutz 108(6): 568–577.
- Arung, E.T, Yoshikawa, K., Shimizu, K. & Kondo, R., 2005. The effect of chlorophorin and its derivative on melanin biosynthesis. Holzforschung 59(5): 514–518.
- Bosu, P.P., Cobbinah, J.R., Nichols, J.D., Nkrumah, E.E. & Wagner, M.R., 2006. Survival and growth of mixed plantations of Milicia excelsa and Terminalia superba 9 years after planting in Ghana. Forest Ecology and Management 233: 352–357.
- Durrieu de Madron, L., 2003. Accroissement diamétrique du bété et de l’iroko. Bois et Forêts des Tropiques 275(1): 83–87.
- Durrieu de Madron, L., Nasi, R. & Détienne, P., 2000. Accroissements diamétriques de quelques essences en forêt dense africaine. Bois et Forêts des Tropiques 263(1): 63–74.
- FAO, 1986. Some medicinal forest plants of Africa and Latin America. FAO Forestry Paper 67. Rome, Italy. 252 pp.
- Farmer, R.H., 1972. Handbook of hardwoods. 2nd Edition. Her Majesty’s Stationery Office, London, United Kingdom. 243 pp.
- Gérard, J., Edi Kouassi, A., Daigremont, C., Détienne, P., Fouquet, D. & Vernay, M., 1998. Synthèse sur les caractéristiques technologiques des principaux bois commerciaux africains. Document Forafri 11. Cirad, Montpellier, France. 185 pp.
- Hawthorne, W.D., 1995. Ecological profiles of Ghanaian forest trees. Tropical Forestry Papers 29. Oxford Forestry Institute, Department of Plant Sciences, University of Oxford, United Kingdom. 345 pp.
- InsideWood, undated. [Internet] http://insidewood.lib.ncsu.edu/search/. May 2007.
- Jøker, D., 2005. Milicia excelsa (Welw.) C.C.Berg. Seed leaflet No 63 (2002, revised 2005). Danida Forest Seed Centre, Humlebaek, Denmark. 2 pp.
- Neuwinger, H.D., 2000. African traditional medicine: a dictionary of plant use and applications. Medpharm Scientific, Stuttgart, Germany. 589 pp.
- Nyong’o, R.N., Cobbinah, J.R. & Appiah-Kwarteng, J., 1994. Flowering and fruiting patterns in Milicia excelsa and Milicia regia Welw. Ghana Journal of Forestry 1: 19–29.
- Ofori, D.A., Cobbinah, J.R. & Appiah-Kwarteng, J., 2001. Genetic variation, heritability and expected genetic gains in Milicia excelsa (iroko). Journal of Tropical Forest Science 13(2): 344–361.
- Ofori, D.A., Newton, A.C., Leakey, R.R.B. & Grace, J., 1997. Vegetative propagation of Milicia excelsa by leafy stem cuttings: effects of maturation, coppicing, cutting length and position on rooting ability. Journal of Tropical Forest Science 10(1): 115–129.
- Olajide, O.A., Kolawole, O.T., Fagbohun, T.R. & Ajayi, F.F., 2005. Evaluation of the anti inflammatory properties of Chlorophora excelsa stem bark extract. Pharmaceutical Biology 43(9): 746–748.
- Ouinsavi, C., Sokpon, N. & Bada, O., 2005. Utilization and traditional strategies of in situ conservation of iroko (Milicia excelsa (Welw.) C.C. Berg) in Benin. Forest Ecology and Management 207(3): 341–350.
- Padayachee, T. & Odhav, B., 2001. Anti-amoebic activity of plant compounds from Virgilia oroboides and Chlorophora excelsa. Journal of Ethnopharmacology 78(1): 59–66.
- Sales, C., 1979. Quelques durées de séchage. Bois et Forêts des Tropiques 186: 52–53.
- Wagner, M.R., Atuahene, S.K.N. & Cobbinah, J.R., 1991. Forest entomology in West Tropical Africa: Forest insects of Ghana. Kluwer Academic Press, Dordrecht, Netherlands. 210 pp.
- White, M.G., 1966. The problem of the Phytolyma gall bug in the establishment of Chlorophora. Institute Paper No 37. Commonwealth Forestry Institute, University of Oxford, Oxford, United Kingdom. 52 pp.
Sources de l'illustration
- Berg, C.C., 1977. Revisions of African Moraceae (excluding Dorstenia, Ficus, Musanga and Myrianthus). Bulletin du Jardin Botanique National de Belgique 47(3–4): 267–407.
- Hawthorne, W., 1990. Field guide to the forest trees of Ghana. Natural Resources Institute, for the Overseas Development Administration, London, United Kingdom. 275 pp.
- Wilks, C. & Issembé, Y., 2000. Les arbres de la Guinée Equatoriale: Guide pratique d’identification: région continentale. Projet CUREF, Bata, Guinée Equatoriale. 546 pp.
Auteur(s)
- D.A. Ofori, Forestry Research Institute of Ghana (FORIG), University P.O. Box 63, KNUST, Kumasi, Ghana
Citation correcte de cet article
Ofori, D.A., 2007. Milicia excelsa (Welw.) C.C.Berg. In: Louppe, D., Oteng-Amoako, A.A. & Brink, M. (Editors). PROTA (Plant Resources of Tropical Africa / Ressources végétales de l’Afrique tropicale), Wageningen, Netherlands. Consulté le 17 décembre 2024.
- Voir cette page sur la base de données Prota4U.