Khaya ivorensis (PROTA)
Introduction |
| Importance générale | |
| Répartition en Afrique | |
| Répartition mondiale | |
| Médicinal | |
| Bois d'œuvre | |
| Bois de feu | |
| Ornemental | |
| Auxiliaire | |
| Statut de conservation | |
Khaya ivorensis A.Chev.
- Protologue: Veg. Ut. Afr. Trop. Franç. 5: 207 (1909).
- Famille: Meliaceae
- Nombre de chromosomes: 2n = 50
Noms vernaculaires
- Acajou rouge, acajou du Gabon, acajou Bassam, acajou à peau rugueuse (Fr).
- Red mahogany, Lagos mahogany (En).
- Acaju de Bassan (Po).
Origine et répartition géographique
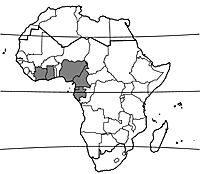
Khaya ivorensis est réparti de la Côte d’Ivoire jusqu’au Cameroun et à Cabinda (Angola) ; il est possible qu’il soit présent aussi en Guinée, au Liberia, en Centrafrique et au Congo. Sa culture en plantations est assez courante sur son aire naturelle de répartition, mais également en Asie et en Amérique tropicales.
Usages
Le bois (noms commerciaux : acajou d’Afrique, African mahogany) est tenu en haute estime en ébénisterie, pour la fabrication de meubles, de boîtes et de coffrets décoratifs, et pour les placages ; il est aussi couramment utilisé pour les encadrements de fenêtres, les panneaux, les portes et les escaliers. Il convient aux constructions légères, aux revêtements de sol légers, à la construction navale, aux châssis de véhicules, aux manches, aux échelles, aux articles de sport, aux instruments de musique, aux jouets, aux bibelots, aux outils de précision, à la sculpture, le tournage et la pâte à papier. L’acajou est très demandé pour la fabrication des fonds ou des éclisses des guitares acoustiques, car on lui prête de bonnes caractéristiques acoustiques. Traditionnellement, le bois est utilisé pour fabriquer des pirogues monoxyles. Il sert de bois de feu et pour la production de charbon de bois.
L’écorce, de saveur amère, est couramment utilisée en médecine traditionnelle. Les décoctions d’écorce se prennent pour traiter la toux, la fièvre et l’anémie, et en usage externe, elles s’appliquent sur les plaies, les écorchures, les ulcères et les tumeurs, ainsi que comme antalgique pour traiter les douleurs rhumatismales et les lumbagos. La pâte de racine s’applique en lavement pour traiter la dysenterie. En usage externe, les jeunes pousses et les feuilles broyées s’appliquent en guise d’antalgique. Les graines sont utilisées pour la production de savon. Dans certains endroits du Nigeria, on conserve les arbres de Khaya ivorensis dans les plantations de cacaoyer pour l’ombrage qu’ils procurent et ultérieurement pour la production de bois d’œuvre.
Production et commerce international
Dans les expéditions de Khaya ivorensis des pays de l’ouest africain destinées à l’export, le bois est mélangé avec d’autres Khaya spp., surtout Khaya anthotheca (Welw.) C.DC. La Côte d’Ivoire a longtemps été le principal exportateur de bois de Khaya : dès 1925, le volume des exportations avoisinait les 10 000 m³ par an ; pendant la période 1965–1974, elles ont dépassé les 1,5 millions de m³ en grumes de Khaya, avec près de 115 000 m³ de bois scié, soit plus que tous les autres pays africains réunis. Depuis cette époque, les quantités ont baissé, mais en 2004, 41 000 m³ de bois scié de Khaya ont été exportés au prix moyen de US$ 397/m³, et 34 000 m³ en 2005 au prix moyen de US$ 439/m³. Le Ghana a exporté 11 000 m³ de bois scié de Khaya en 2003 au prix moyen de US$ 714/m³, 14 000 m³ en 2004 au prix moyen de US$ 527/m³, et 17 000 m³ en 2005 au prix moyen de US$ 755/m³. Les exportations ghanéennes de placages de Khaya se sont élevées à 4000 m³ en 2003 au prix moyen de US$ 443/m³, 6000 m³ en 2004 au prix moyen de US$ 1677/m³, et 5000 m³ en 2005 au prix moyen de US$ 1938/m³. Dans ces quantités, la proportion de Khaya ivorensis n’est pas bien définie. Le Cameroun a exporté 11 000 m³ de bois scié de Khaya en 2003, et 8600 m³ en 2004 et 2006. Les exportations de grumes du Gabon s’élevaient à 21 300 m³ en 2000, à 18 700 m³ en 2001, 14 300 m³ en 2002, 17 800 m³ en 2003, et 18 600 m³ en 2004. Au cours des dernières années, le marché nord-américain a dominé le commerce mondial de bois d’œuvre de Khaya, notamment pour remplacer l’acajou américain (issu de Swietenia) dont la disponibilité a considérablement chuté.
Propriétés
Le bois de cœur est brun rosé pâle à rouge pâle, et fonce pour prendre une teinte brun foncé lustrée d’or à l’exposition. Il se démarque plus ou moins nettement de l’aubier, blanc crème, dont la largeur atteint 5 cm. Il est contrefil ou à fil droit, le grain est assez grossier.
C’est un bois de poids moyen avec une densité de (420–)460–570 kg/m³ à 12% d’humidité. Il se sèche généralement sans problème à l’air ou au four avec peu de déformation, mais un gauchissement dû à la présence de contrefil peut se produire. Les taux de retrait du bois vert à anhydre sont moyens : de 2,2–4,1%(–5,0)% radialement et 5,0–6,9(–8,4)% tangentiellement. Une fois sec, le bois est relativement stable en service.
A 12% d’humidité, le module de rupture est de 71–126 N/mm², le module d’élasticité de 8700–10 800 N/mm², la compression axiale de 37–48 N/mm², la compression transversale de 4–8 N/mm², le cisaillement de 8–12 N/mm², le fendage de 10–17 N/mm, la dureté Janka de flanc de 3210–3700 N et la dureté Janka en bout de 4810 N.
Le bois est habituellement assez facile à scier et à travailler, mais la présence du contrefil peut être source de difficultés. Il faut par conséquent utiliser des scies affûtées en permanence pour éviter un fini laineux, et un angle d’attaque de 15–20° est recommandé. On peut obtenir un fini lisse, mais le recours à un apprêt est nécessaire pour la teinture et le vernissage. Le bois supporte bien le clouage et le vissage et se colle de façon satisfaisante. Les caractéristiques de cintrage sont médiocres. Facile à dérouler et à trancher, le bois produit des placages d’excellente qualité. Il se tourne relativement bien. La sciure peut provoquer une irritation de la peau.
C’est un bois moyennement durable, qui peut être sensible aux attaques de termites et de foreurs. Le bois de cœur est fortement rebelle à l’imprégnation, l’aubier est moyennement rebelle. Le bois convient à l’industrie papetière, et même les noyaux de déroulage, souvent considérés comme des déchets, peuvent être transformés en pâte.
On a isolé des limonoïdes de l’écorce et des graines. Certains ont eu une activité anti-appétante significative sur les insectes, et une certaine activité antifongique et antibactérienne. Des extraits d’écorce ont manifesté une faible activité antitrypanosome et antiplasmodium dans des essais sur des souris. D’autres essais menés sur des rats ont montré que l’écorce avait une activité anti-inflammatoire dose-dépendante et qu’elle n’était toxique qu’à fortes doses. L’écorce a fait preuve d’effets anticonvulsivants chez les souris. Les graines contiennent 17–27% d’huile, dont les acides gras dominants sont l’acide palmitique, l’acide oléique et l’acide linoléique. Une autre analyse a fait ressortir une teneur en huile d’environ 48% à 7% d’humidité, ainsi que la composition en acides gras suivante : acide palmitique 7%, acide stéarique 32%, acide oléique 15% et acide linoléique 45%. L’huile peut servir d’additif dans les savons liquides, et la présence de limonoïdes comme le méthylangolensate lui permet de jouer le rôle d’antibactérien et d’antifongique. Au Nigeria, des études ont montré que l’écorce contenait 27% de tanins extractibles. La fumée du bois a donné de bons résultats dans des essais de fumage du poisson, auquel elle offre une protection efficace contre les champignons.
Falsifications et succédanés
Le bois de Khaya anthotheca est très similaire à celui de Khaya ivorensis. Dans les expéditions d’Afrique de l’Ouest destinées à l’exportation, ces essences sont mélangées au bois de Khaya grandifoliola C.DC sous la dénomination “acajou d’Afrique” ou “African mahogany”. Le bois de makoré (Tieghemella) lui ressemble mais il est plus durable.
Description
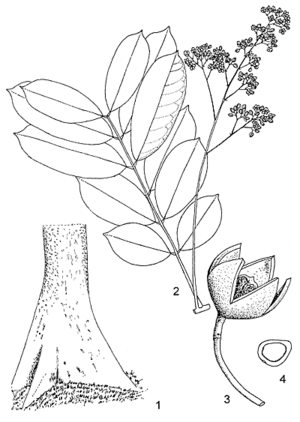
- Arbre monoïque, sempervirent ou caducifolié, de taille grande à très grande, atteignant 60 m de haut ; fût dépourvu de branches sur 30 m, habituellement droit et cylindrique, atteignant 160(–210) cm de diamètre, à grands contreforts atteignant 2(–4) m de haut, se prolongeant parfois en racines superficielles proéminentes ; surface de l’écorce brune et légèrement rugueuse, s’exfoliant en petites écailles circulaires laissant une surface grêlée, marbrée de brun grisâtre et de brun orangé, écorce interne rose à rougeâtre ; cime massive, arrondie ; rameaux glabres.
- Feuilles disposées en spirale mais groupées vers l’extrémité des branches, composées paripennées à (3–)4–7 paires de folioles ; stipules absentes ; pétiole de 1–4 cm de long, rachis de 6–20 cm long ; pétiolules de 0,5–1 cm de long ; folioles opposées, oblongues à oblongues-elliptiques, de 5–14 cm × 2–6 cm, cunéiformes à obtuses et légèrement asymétriques à la base, distinctement acuminées à l’apex, à bords entiers, coriaces, glabres, pennatinervées à 5–10 paires de nervures latérales.
- Inflorescence : panicule axillaire atteignant 20 cm de long.
- Fleurs unisexuées, fleurs mâles et femelles d’aspect très similaire, régulières, (4–)5-mères, blanchâtres, au parfum doux ; pédicelle de 1–3 mm de long ; calice lobé presque jusqu’à la base, à lobes arrondis d’environ 1 mm de long ; pétales libres, elliptiques, d’environ 4 mm × 2 mm, légèrement cucullés ; étamines soudées en un tube urcéolé d’environ 5 mm de long, à (8–)10 anthères incluses à proximité de l’apex, alternant avec les lobes arrondis ; disque en coussin ; ovaire supère, globuleux à conique, de 1–2 mm de diamètre, 5-loculaire, style atteignant 1 mm de long, stigmate discoïde ; fleurs mâles à ovaire rudimentaire, fleurs femelles à anthères plus petites indéhiscentes.
- Fruit : capsule ligneuse, érigée, presque globuleuse, de 5–7 cm de diamètre, brun grisâtre, déhiscente par 5 valves, contenant de nombreuses graines.
- Graines discoïdes ou quadrangulaires, fortement aplaties, de 2–2,5 cm × 2,5–3,5 cm, étroitement ailées à la périphérie, brunes.
- Plantule à germination hypogée, cotylédons restant enfermés dans le tégument ; épicotyle de 5–10 cm de long ; 2 premières feuilles opposées, simples.
Autres données botaniques
Le genre Khaya comprend 4 espèces sur le continent africain et 1 ou 2 endémiques des Comores et de Madagascar. Il appartient à la sous-famille des Swietenoideae et semble être étroitement apparenté à Carapa et Swietenia. Les espèces de Khaya ont de fortes ressemblances au niveau des fleurs et des fruits, les différences les plus nettes résidant dans leurs folioles. Il semble y avoir une transition plus ou moins graduelle des espèces, en suivant les gradients écologiques, depuis la zone de forêt humide sempervirente, jusqu'à la forêt semi-décidue et à la zone de savane. Les études sur les propriétés anatomiques, chimiques et physiques du bois ont confirmé la grande proximité des espèces de Khaya, les principales différences résidant dans le ratio lumen/paroi des fibres, le pourcentage de rayons multisériés et la densité du bois, qui pourraient aussi s’expliquer, au moins en partie, par les conditions écologiques. Khaya anthotheca (Welw.) C.DC. est très proche de Khaya ivorensis, mais s’en distingue, outre ses besoins écologiques, par ses folioles plus ovales-elliptiques et courtement acuminées et son écorce plus lisse de couleur claire.
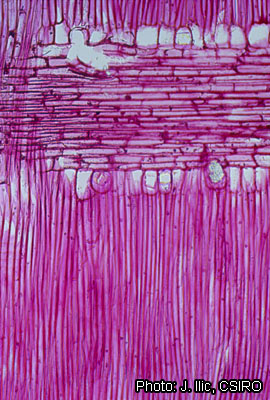
Anatomie
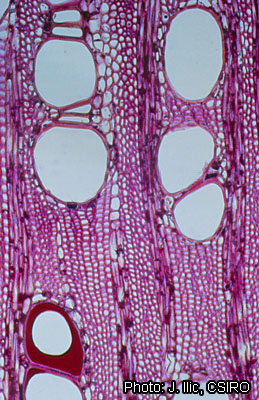
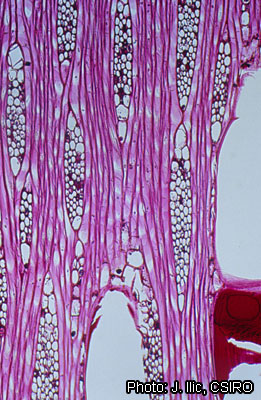
Description anatomique du bois (codes IAWA pour les bois feuillus) :
- Cernes de croissance : 2 : limites de cernes indistinctes ou absentes.
- Vaisseaux : 5 : bois à pores disséminés ; 13 : perforations simples ; 22 : ponctuations intervasculaires en quinconce ; 23 : ponctuations alternes (en quinconce) de forme polygonale ; 24 : ponctuations intervasculaires minuscules (très fines) (≤ 4μm) ; 30 : ponctuations radiovasculaires avec des aréoles distinctes ; semblables aux ponctuations intervasculaires en forme et en taille dans toute la cellule du rayon ; 42 : diamètre tangentiel moyen du lumen des vaisseaux 100–200 μm ; (43 : diamètre tangentiel moyen du lumen des vaisseaux ≥ 200 μm) ; 46 : ≤ 5 vaisseaux par millimètre carré ; 47 : 5–20 vaisseaux par millimètre carré ; 58 : gomme ou autres dépôts dans les vaisseaux du bois de cœur.
- Trachéides et fibres : 61 : fibres avec des ponctuations simples ou finement (étroitement) aréolées ; (65 : présence de fibres cloisonnées) ; 66 : présence de fibres non cloisonnées ; 69 : fibres à parois fines à épaisses.
- Parenchyme axial : 78 : parenchyme axial juxtavasculaire ; 79 : parenchyme axial circumvasculaire (en manchon) ; (89 : parenchyme axial en bandes marginales ou semblant marginales) ; 93 : huit (5–8) cellules par file verticale.
- Rayons : 98 : rayons couramment 4–10-sériés ; (103 : rayons de deux tailles différentes) ; 106 : rayons composés de cellules couchées avec une rangée terminale de cellules dressées et/ou carrées ; 107 : rayons composés de cellules couchées avec 2 à 4 rangées terminales de cellules dressées et/ou carrées ; 115 : 4–12 rayons par mm.
- Eléments sécrétoires et variantes cambiales : 131 : canaux intercellulaires d’origine traumatique.
- Inclusions minérales : 136 : présence de cristaux prismatiques ; 137 : cristaux prismatiques dans les cellules dressées et/ou carrées des rayons ; (140 : cristaux prismatiques dans les cellules cloisonnées, dressées et/ou carrées des rayons).
Croissance et développement
Dans des pépinières de Côte d’Ivoire, les semis de Khaya ivorensis âgées de 1 an faisaient 90–100 cm de haut, les gaulis de 2 ans de 2,5–3 m de haut, les gaulis de 4 ans de 4–6 m, et les gaulis de 6 ans atteignaient 12–15 m de haut et 10–18 cm de diamètre. Des individus plantés dans des endroits dégagés de la zone de forêt sempervirente avaient atteint une hauteur moyenne de 12 m et un diamètre de fût moyen de 15 cm au bout de 8 ans. Dans des plantations mixtes, le diamètre de fût moyen était de 39 cm au bout de 27 ans, les individus dominants faisant 28 m de haut et 47 cm de diamètre. A 34 années après la plantation, les arbres dominants atteignaient 76 cm de diamètre, mais le fût n’était dépourvu de branches que sur 12 m. Au Nigeria, la hauteur moyenne des gaulis était de 4,5 m au bout de 4 années, avec un diamètre moyen du tronc de 8 cm. Dans des plantations de 26 ans en Malaisie, l’accroissement annuel moyen atteint était de 1,8 cm de diamètre et 1 m de hauteur. Dans une plantation âgée de 40 ans en Malaisie, la hauteur moyenne des arbres était de 23,5 m et le diamètre de fût moyen de 29,5 cm, et chez les individus dominants de 30 m et 47 cm, respectivement. Chez les spécimens jeunes, le tronc est élancé et la cime petite. Une importante croissance latérale débute lorsque la canopée supérieure de la forêt a été atteinte. L’arbre se développe selon le modèle architectural de Rauh, caractérisé par un tronc monopodial qui grandit de façon rythmique et où les branches se déploient par étages successifs. L’état monoaxial peut se maintenir sur une hauteur de 10 m.
Les arbres sont parfois sans feuilles pendant une brève période au début de la saison sèche. Dans les forêts sempervirentes humides, on trouve des individus de Khaya ivorensis qui fleurissent et fructifient toute l’année et qui ont des fleurs et des fruits en même temps, mais habituellement la floraison est saisonnière ; en Afrique de l’Ouest, elle est surtout abondante en juin–octobre. Les fruits mûrissent en 6 mois environ. En Côte d’Ivoire, il y a généralement deux périodes de fructification : février–avril et juillet–août ; au Ghana, la principale période de fructification est en février–mai. Des arbres âgés de 30 ans peuvent produire des fruits et des graines en abondance. Il y aurait une production massive de graines tous les 3–4 ans. La dispersion des graines se fait par le vent, mais la plupart tombent dans le périmètre immédiat de l’arbre-mère.
Ecologie
Khaya ivorensis abonde surtout dans la forêt sempervirente, mais on le trouve aussi dans la forêt semi-décidue humide, dans les régions ayant une pluviométrie annuelle de 1600–2500 mm et une saison sèche de 2–3 mois, jusqu’à 700 m d’altitude. Dans la forêt semi-décidue humide, il peut coexister avec Khaya anthotheca. Khaya ivorensis est souvent présent le long des cours d’eau. Il préfère les sols alluviaux humides et bien drainés, mais on le trouve aussi sur les pentes sur latérite. Les graines sont tout aussi capables de germer en plein soleil qu’à l’ombre, mais la régénération naturelle semble rare dans les trouées forestières importantes. Les semis peuvent survivre dans une pénombre dense, mais pour une bonne croissance, ils ont besoin d’ouvertures dans la canopée forestière. La régénération de Khaya ivorensis n’est pas favorisée par des perturbations importantes dans la forêt, mais elle tire profit de petites trouées.
Multiplication et plantation
Khaya ivorensis se multiplie par graines. Le poids de 1000 graines est de 130–310 g. Les graines sont souvent déjà la proie des insectes quand elles sont encore sur l’arbre ; il faut donc procéder à une sélection des semences intactes avant de semer. La température optimale pour le stockage des graines serait de 3°C et le taux d’humidité de 6%. Un semis en planches de pépinière est préférable. La levée, relativement lente, prend 11–40 jours. Le taux de germination de semences fraîches saines est élevé, avoisinant les 100%, mais il décroît rapidement et après 3 mois, la viabilité des graines n’est plus que de 5%. En pépinière, un léger ombrage avantage les semis jusqu’à 2 ans ; cela permet de réduire les attaques du foreur des pousses Hypsipyla et le développement de galles sur les feuilles. Une application de 0,5 g d’engrais minéral sur les semis est recommandé, car il favorise la croissance en hauteur et celle du diamètre au collet. Les semis se repiquent lorsqu’ils atteignent 60–90 cm de haut, habituellement sous la forme de stumps ou de plants effeuillés.
Une propagation végétative expérimentale au moyen de boutures de semis de moins de 2 ans a réussi avec une application d’auxine (AIB) à une concentration de 200 μg par bouture. Les boutures issues de nœuds de la base ont mieux pris que celles des nœuds apicaux, les boutures longues (de 4 cm de long) mieux que les courtes (2 cm), et par ailleurs, un éclaircissage de la surface foliaire jusqu’à 10 cm² a également favorisé l’enracinement.
En Côte d’Ivoire, la première plantation de Khaya ivorensis a été établie en 1927, à la densité de 2500 plants/ha, mais après 30 ans, seuls 72 arbres/ha présentaient une croissance annuelle en diamètre de plus de 1 cm. Par la suite, il a été planté en lignes pour enrichir les forêts dégradées, en mélange avec d’autres essences, à une distance de 7–25 m entre les lignes et de 3–7 m sur la ligne, et certains individus présentaient une croissance annuelle du diamètre de plus de 2,5 cm après 14 ans. Entre 1969 et 1995, environ 1730 ha de plantations pures ont été établies, en espaçant les arbres de 3 m × 3 m. Plus récemment, il a été planté avec succès en triples rangs pour marquer la limite des réserves forestières.
Gestion
Khaya ivorensis est présent de façon disséminée ou en petits groupes dans la forêt, généralement en faibles densités. Dans le sud du Cameroun, on a observé en moyenne 0,02–0,08 fûts de plus de 60 cm de diamètre à l’ha et un volume de 0,17–0,64 m³ de bois à l’ha ; au Gabon, la moyenne s’élevait à 0,27 m³ de bois à l’ha. Pour la Côte d’Ivoire, on a pu constater une densité moyenne de moins de 1 arbre exploitable pour 10 ha, mais on a trouvé par endroits 1 arbre exploitable pour 2 ha.
Des plantations d’enrichissement de la forêt naturelle se pratiquent dans certains endroits de la Côte d’Ivoire. Au Gabon, des semis de 4 mois ont été plantés après des coupes à blanc de la forêt, et sur d’autres sites après avoir ôté la végétation de sous-bois et éclairci la canopée supérieure. Après 6 ans, les semis présentaient 92% de survie dans les endroits soumis aux coupes à blanc et près de 100% dans des endroits où la forêt avait été débarrassée de sa végétation de sous-bois et la canopée éclaircie. La hauteur moyenne était de 10,7 m et de 11,7 m, respectivement, et le diamètre de fût moyen de 12,9 cm et 9,3 cm. Au bout de 11 ans, la hauteur moyenne des arbres était de 16,1 m et 17,1 m, respectivement, et le diamètre de fût moyen de 43,1 cm et 36,5 cm.
En Côte d’Ivoire, des arbres de Khaya ivorensis ont été plantés à l’ombre de Leucaena leucocephala (Lam.) de Wit âgés de 2 ans, espèce qui empêche les adventices de pousser et fixe l’azote dans le sol. Il est nécessaire de procéder à une éclaircie régulière des arbres d’ombrage dans les premières années pour que Khaya ivorensis pousse bien. La première éclaircie dans une plantation de Khaya ivorensis comprenant 1000 tiges/ha est effectuée lorsque les arbres ont atteint 15 m de haut et 15 cm de diamètre de fût, visant une densité de 400–500 tiges/ha. La deuxième peut être effectuée lorsque les arbres font 20 m de haut et 20 cm de diamètre visant 200–250 tiges/ha, la troisième éclaircie à 25 m de haut et 25 cm de diamètre visant 125–150 tiges/ha, et la quatrième à 30 cm de diamètre visant 75–100 tiges/ha. En Afrique tropicale, Khaya ivorensis a été planté avec succès en plantations mixtes, par ex. avec Heritiera utilis (Sprague) Sprague, Terminalia ivorensis A.Chev., Tieghemella heckelii (A.Chev.) Roberty et Triplochiton scleroxylon K.Schum. En Malaisie, dans les plantations mixtes comportant Khaya ivorensis, une densité ultime de 80 arbres/ha et des rotations sur 30 ans sont recommandées. Mais dans la forêt naturelle, les cycles de rotation réalistes sont probablement de l’ordre de 60–80 ans.
Maladies et ravageurs
Dans les plantations, Khaya ivorensis peut être sérieusement affecté par le foreur des pousses Hypsipyla robusta qui tue la tige principale des jeunes arbres, les poussant à une ramification excessive et contribuant à leur mortalité. Les dégâts qu’il cause peuvent être limités par des techniques sylvicoles telles que l’ombrage par le haut des gaulis, la plantation mixte et l’ablation des pousses latérales. Au Nigeria, dans les années 1960 par exemple, on a découvert que les foreurs des pousses touchaient 90–100% d’individus dans des peuplements purs de Khaya ivorensis, 0–30% dans des peuplements mélangés avec d’autres Meliaceae, 0–50% dans des peuplements mélangés avec des non-Meliaceae et 0% dans des plantations en lignes en forêt naturelle. Au Brésil, Khaya ivorensis est utilisé pour le reboisement en raison de sa résistance à Hypsipyla grandella, le principal ravageur de l’acajou brésilien. Cependant, depuis 1999, une forte incidence de taches foliaires provoquées par le champignon Thanatephorus cucumeris (teléomorphe de Rhizoctonia solani) a été observée, provoquant de nombreuses lésions sur les feuilles des arbres de grande taille et la chute des feuilles à 100% chez les semis.
Les graines sont couramment attaquées par les coléoptères foreurs de graines et consommées par les petits rongeurs. Des attaques d’arbres vivants par des xylophages (Apate spp.) ont été observées. Les porcs-épics et les écureuils dévorent parfois l’écorce des gaules, ce qui peut tuer la plante. Dans les pépinières ivoiriennes, les semis sont fréquemment la proie des psylles (Phacosema spp.), des punaises et des cochenilles, avant d’être infestées par des agents pathogènes fongiques secondaires, ce qui se traduit par un charbon qui noircit les feuilles.
Récolte
Le diamètre de fût minimum pour l’exploitation est de 60 cm en Côte d’Ivoire et au Gabon, de 80 cm au Cameroun et de 110 cm au Ghana. Les fûts de Khaya ivorensis sont parfois si gros qu’ils ne peuvent être sciés avec l’outillage habituel. Les hauts contreforts à la base des fûts nécessitent souvent la construction d’une plateforme, ou leur suppression pure et simple avant l’abattage afin de récupérer davantage de bois.
Rendement
Un individu poussant en forêt naturelle ayant un diamètre de fût de 80 cm donne un rendement moyen de 6,6 m³ de bois, un arbre de 120 cm de diamètre 15,5 m³, et un arbre de 160 cm de diamètre 17,9 m³.
Pour les plantations âgées de 30 ans en Afrique tropicale, la production annuelle de bois est de 2–4 m³/ha. Sur un bon sol en Côte d’Ivoire, un peuplement âgé de 31 ans avec 70 arbres/ha (d’en moyenne 37–40 m de haut et 57 cm de diamètre) a produit 8 m³/ha/an. Dans des plantations de 26–28 ans en Malaisie, des accroissements annuels moyens de 7,4–7,7 m³/ha ont été enregistrés.
Traitement après récolte
Les grumes ont parfois un cœur spongieux ou cassant qui impose la prudence dans les opérations d’abattage et de sciage. Elles sont sensibles aux attaques de capricornes et il ne faut pas trop attendre après l’abattage pour entamer la transformation. L’aubier est souvent extrait peu de temps après l’abattage pour prévenir les attaques de scolytes. Les fûts ne coulent pas et leur flottage est donc possible.
Ressources génétiques
Khaya ivorensis figure sur la Liste rouge de l’UICN en tant qu’espèce vulnérable en raison de la perte et de la dégradation de son milieu, ainsi que de son abattage sélectif. Son inscription à l’annexe I ou II de la CITES a été proposée, mais l’insuffisance d’informations relatives à sa régénération, à l’étendue des plantations et à sa durabilité avec les méthodes de gestion actuelles l’a écarté de la liste.
Sélection
Des essais de provenances au Ghana ont mis en évidence une héritabilité assez élevée de la croissance en hauteur : en effet, les descendants qui arrivaient en tête faisaient le double de hauteur de ceux classés derniers. Cela peut s’expliquer en partie par une certaine résistance génétique aux attaques de Hypsipyla robusta. Des essais de provenances ont été plantés également en Côte d’Ivoire.
Perspectives
La régénération naturelle de Khaya ivorensis après la coupe est souvent médiocre en raison de la densité souvent faible des arbres mûrs dans la forêt et les faibles taux de régénération dans les forêts fortement perturbées. On a émis l’hypothèse qu’un ajout de semences dans des sites favorables était une possibilité réaliste d’obtenir une régénération suffisante après la coupe. Un approfondissement des recherches est nécessaire sur des systèmes de gestion appropriés en forêt naturelle pour assurer une exploitation durable. Une gestion conforme au système tropical de régénération par coupes progressives semble tout à fait appropriée.
Khaya ivorensis est considéré comme l’une des plus importantes essences de bois d’œuvre pour les plantations, car elle associe croissance rapide et bois de bonne qualité. L’établissement de plantations de Khaya ivorensis à plus vaste échelle en Afrique tropicale est sans nul doute souhaitable, mais les attaques de Hypsipyla sont un sérieux inconvénient. Les effets combinés d’une sélection de provenances apportant une résistance génétique et de méthodes sylvicoles appropriées pourraient avoir un impact positif considérable sur les dégâts causés par les foreurs de tige Hypsipyla robusta. L’intégration de Khaya ivorensis dans des systèmes d’agroforesterie, comme c’est déjà le cas de ceux reposant sur le cacao au Nigeria, peut être considérée réalisable sur les plans économique et technique et constitue une stratégie saine du point de vue écologique.
Il est recommandé de procéder à des études biosystématiques sur Khaya couvrant toute l’aire du genre et tenant compte en outre des besoins écologiques.
Références principales
- Bolza, E. & Keating, W.G., 1972. African timbers: the properties, uses and characteristics of 700 species. Division of Building Research, CSIRO, Melbourne, Australia. 710 pp.
- Burkill, H.M., 1997. The useful plants of West Tropical Africa. 2nd Edition. Volume 4, Families M–R. Royal Botanic Gardens, Kew, Richmond, United Kingdom. 969 pp.
- CTFT (Centre Technique Forestier Tropical), 1979. Acajou d’Afrique. Bois et Forêts des Tropiques 183: 33–48.
- Dupuy, B. & M’Bla Koua, 1993. Les plantations d’acajou d’Afrique: leur sylviculture en forêt dense humide ivoirienne. Bois et Forêts des Tropiques 236: 25–42.
- Laryea, S.K., 2005. Soap from Khaya ivorensis seed oil. B.Sc. Chemistry degree thesis, Department of Chemistry, Faculty of Science, University of Cape Coast, Cape Coast, Ghana. 44 pp.
- Ofori, D.A., Opuni-Frimpong, E. & Cobbinah, J.R., 2007. Provenance variation in Khaya species for growth and resistance to shoot borer Hypsipyla robusta. Forest Ecology and Management 242: 438–443.
- Opuni-Frimpong, E., 2006. Improving productivity and conservation of African mahogany: genetic selection, propagation and silvicultural management of Hypsipyla robusta (Moore). PhD Forest Science degree thesis, School of Forest resources and Environmental Science, Michigan Technological University, Houghton, United States. 177 pp.
- Phongphaew, P., 2003. The commercial woods of Africa. Linden Publishing, Fresno, California, United States. 206 pp.
- Styles, B.T. & White, F., 1991. Meliaceae. In: Polhill, R.M. (Editor). Flora of Tropical East Africa. A.A. Balkema, Rotterdam, Netherlands. 68 pp.
- Takahashi, A., 1978. Compilation of data on the mechanical properties of foreign woods (part 3) Africa. Shimane University, Matsue, Japan, 248 pp.
Autres références
- Abdelgaleil, A.A.M., Hashinaga, F. & Nakatani, M., 2005. Antifungal activity of limonoids from Khaya ivorensis. Pest Management Science 61(2): 186–190.
- Agbedahunsi, J.M., Fakoya, F.A. & Adesanya, S.A., 2004. Studies on the anti-inflammatory and toxic effects of the stem bark of Khaya ivorensis (Meliaceae) on rats. Phytomedicine 11(6): 504–508.
- Atindehou, K.K., Schmid, C., Brun, R., Koné, M.W. & Traoré, D., 2004. Antitrypanosomal and antiplasmodial activity of medicinal plants from Côte d’Ivoire. Journal of Ethnopharmacology 90(2): 221–227.
- Billand, A., 1987. Inventaire des dispositifs d’amélioration génétique de cédréla, cordia, fraké, framiré, gmélina, teck, acajou au CTFT de Côte d’Ivoire. Centre Technique Forestier Tropical de Côte d’Ivoire, Abidjan, Côte d’Ivoire. 95 pp.
- CIRAD Forestry Department, 2003. Acajou d’Afrique. [Internet] Tropix 5.0. http://tropix.cirad.fr/africa/acajou.pdf. January 2008.
- de Koning, J., 1983. La forêt de Banco. Part 2: La Flore. Mededelingen Landbouwhogeschool Wageningen 83–1. Wageningen, Netherlands. 921 pp.
- Donkor, B.N., 1997. Stem wood structure of four Ghanaian Khaya species. M.Sc. Forestry thesis, Faculty of Forestry, Lakehead University, Thunder Bay, Ontario, Canada. 92 pp.
- Hawthorne, W.D., 1995. Ecological profiles of Ghanaian forest trees. Tropical Forestry Papers 29. Oxford Forestry Institute, Department of Plant Sciences, University of Oxford, United Kingdom. 345 pp.
- InsideWood, undated. [Internet] http://insidewood.lib.ncsu.edu/search/. May 2007.
- Keay, R.W.J., 1989. Trees of Nigeria. A revised version of Nigerian trees (1960, 1964) by R.W.J. Keay, C.F.A. Onochie and D.P. Stanfield. Clarendon Press, Oxford, United Kingdom. 476 pp.
- Koumba Zaou, P., Mapaga, D., Nze Nguema, S. & Deleporte, P., 1998. Croissance de 13 essences de bois d’oeuvre plantées en forêt Gabonaise. Bois et Forêts des Tropiques 256(2): 21–32.
- Mallet, B. & Berthault, J-G., 1990. Croissance de l’acajou bassam, Khaya ivorensis, en basse Côte d’Ivoire. Centre Technique Forestier Tropical de Côte d’Ivoire, Abidjan, Côte d’Ivoire. 12 pp.
- Neuwinger, H.D., 2000. African traditional medicine: a dictionary of plant use and applications. Medpharm Scientific, Stuttgart, Germany. 589 pp.
- Odigie, G.A., 1983. Field growth of some mahogany species in the tropical rainforest area of Nigeria. Nigerian Agricultural Journal 13: 25–29.
- Raponda-Walker, A. & Sillans, R., 1961. Les plantes utiles du Gabon. Paul Lechevalier, Paris, France. 614 pp.
- Roberts, H., 1965. A survey of the important shoot, stem, wood, flower and fruit boring insects of the Meliaceae in Nigeria. Nigerian Forestry Information Bulletin (New Series) No 15. Federal Ministry of Information, Lagos, Nigeria. 38 pp.
- Siepel, A., Poorter, L. & Hawthorne, W.D., 2004. Ecological profiles of large timber species. In: Poorter, L., Bongers, F., Kouamé, F.N. & Hawthorne, W.D. (Editors). Biodiversity of West African forests. An ecological atlas of woody plant species. CABI Publishing, CAB International, Wallingford, United Kingdom. pp. 391–445.
- Tchoundjeu, Z. & Leakey, R.R.B., 1996. Vegetative propagation of African mahogany: effects of auxin, node position, leaf area and cutting length. New Forests 11(2): 125–136.
- Vanucci, C., Lange, C., Lhommet, G., Dupont, B., Davoust, D., Vauchot, B., Clement, J.L. & Brunck, F., 1992. An insect antifeedant limonoid from seed of Khaya ivorensis. Phytochemistry 31(9): 3003–3004.
- Vivien, J. & Faure, J.J., 1985. Arbres des forêts denses d’Afrique Centrale. Agence de Coopération Culturelle et Technique, Paris, France. 565 pp.
- Wiselius, S.I., 1998. Khaya A. Juss. In: Sosef, M.S.M., Hong, L.T. & Prawirohatmodjo, S. (Editors). Plant Resources of South-East Asia No 5(3). Timber trees: Lesser-known timbers. Backhuys Publishers, Leiden, Netherlands. pp. 310–313.
Sources de l'illustration
- Aubréville, A., 1959. La flore forestière de la Côte d’Ivoire. Deuxième édition révisée. Tome deuxième. Publication No 15. Centre Technique Forestier Tropical, Nogent-sur-Marne, France. 341 pp.
- Wilks, C. & Issembé, Y., 2000. Les arbres de la Guinée Equatoriale: Guide pratique d’identification: région continentale. Projet CUREF, Bata, Guinée Equatoriale. 546 pp.
Auteur(s)
- R.H.M.J. Lemmens, PROTA Network Office Europe, Wageningen University, P.O. Box 341, 6700 AH Wageningen, Netherlands
Citation correcte de cet article
Lemmens, R.H.M.J., 2008. Khaya ivorensis A.Chev. In: Louppe, D., Oteng-Amoako, A.A. & Brink, M. (Editors). PROTA (Plant Resources of Tropical Africa / Ressources végétales de l’Afrique tropicale), Wageningen, Netherlands. Consulté le 6 avril 2025.
- Voir cette page sur la base de données Prota4U.